アメリカ国立衛生研究所(NIH)合意会議(1980)による熱性けいれんの定義
“生後3ヶ月から5歳の乳幼児によくみられる、頭蓋内感染などのけいれん誘発性疾患を原因としない、発熱をともなう発作。無熱性けいれんの既往のある子どもに発熱にともなってけいれんがみられても熱性けいれんとはいわない”
日本小児神経学会 熱性けいれん診療ガイドライン改定ワーキンググループ(2023)による熱性けいれんの定義
“おもに生後満6か月から満60か月までの乳幼児期に起こる、通常は38℃以上の発熱に伴う発作性疾患(けいれん性、非けいれん性を含む)で、髄膜炎などの中枢神経感染症、代謝異常、その他の明らかな発作の原因がみられないもので、てんかんの既往のあるものは除外される”
内容
アメリカ国立衛生研究所(NIH)合意会議(1980)による熱性けいれんの定義
日本小児神経学会 熱性けいれん診療ガイドライン改定ワーキンググループ(2023)熱性けいれん(熱性発作)診療ガイドラインの熱性けいれんの定義
未解決の問題――熱性けいれん重積発作と内側側頭葉硬化てんかん.
熱性けいれんQ&A集
| 質問 | 答え |
| 熱性けいれんとは何ですか? | 乳幼児のお子さんによくみられる熱をともなってみられるけいれんのことです。 けいれんの多くは発熱後24時間以内にみられ、ほとんどが、数十秒で終わってしまいます。ただし、まれに、20分以上続くことがあります。 日本では熱性けいれんは乳幼児期のお子さん100人のうち数人が1回は経験する、きわめてありふれた疾患です。 |
| 熱にともなってけいれんがみられても熱性けいれんとはいわない病気にはどんなものがありますか。 | 脳炎、細菌性髄膜炎といった中枢神経感染症、あるいは、発熱をともなう下痢や嘔吐で脱水になったり、塩分バランスが崩れたりして起きるけいれんは熱性けいれんとはいいません。 てんかんのお子さんが発熱してけいれんを起こした場合も熱性けいれんとは考えません。 |
| 熱性けいれんの熱にはなにか特徴がありますか? | 多くが高熱です。39℃以上の高熱が特徴の突発性発疹症では熱性けいれんが起きやすいことが知られています。 しかし、けいれんの引き金となるのが熱の高さなのか、熱の上昇スピードなのか、熱に対する体内反応なのか、まだ、よくわかっていません。 |
| 熱性けいれんではどんな症状がみられますか? | 熱性けいれんがおきると、意識を失い、反応しなくなります。体をこわばらせ、四肢をふるわせます。吐いたり、失禁したりすることもあります。たいてい、けいれん症状は左右対称です。 しかし、まれに、左右いずれか一方の症状が強いことがあります。また、発作前、一瞬、ボーッとしていることもあります。 けいれんが止まった後、数十分、ボンヤリして、おかしな動作をすることが、ときとしてみられます。しかし、そうした異常運動の多くは発作後のもうろう状態によるもので、けいれんとは別物です。 |
| けいれんの時、やるべきこと、やるべきでないことを教えて下さい。 | とにかく、落ち着いて下さい。 首が締めつけられないよう服をゆるめ、安全な場所に顔を横にして寝かせてあげてください。できれば,時刻を確認し,発作の始まりから終わりまでの時間と発作の症状を書きとめてください。 強く抱きしめたり、押さえつけたりして、けいれんを止めようなどとは考えないでください。けいれんは力ずくで止まるものではありません。 舌を咬むのを恐れて口に何か突っ込むようなことはしないでください。舌を咬むのは発作の始まりのときがほとんどです。発作が始まってから何かしても手遅れです。口に何か突っ込むと、口の中を傷つけたり、窒息させたりする恐れがあり、かえって危険です。 |
| 熱は下げるべきですか? | 発作がおさまったら、まずは、熱を下げることを考えましょう。熱を下げる座薬(アセトアミノフェン系:アンヒバ、アルピニー、カロナールなど)が手元にあれば、おしりに入れてあげて下さい。 ただし、解熱剤は発熱からくる不快感,食欲低下などの軽減には有効ですが,けいれんにたいする予防効果はなく、発作の再発をおさえることはできません。 |
| 熱性けいれんでは起こらない、といえることは、どんなことですか? | 短いけいれん(10分以内)で死亡したり、脳が傷ついたりすることは、まず、ありません。早死にすることも、病弱になることもありません。 熱性けいれんが原因で、てんかんになったり、知能が低下したり、学業が不振に陥ることもほとんどありません。 |
| 熱がでると、また、ひきつけるのですか? | 3分の2のお子さんは2度と発作を起こすことはありません.熱をだしたとき再び発作を起こす可能性のあるのは3人に1人のお子さんだけです。3回目の発作を起こすお子さんはもっと少なく、10人に1人です。 家族のどなたかに熱性けいれんの既往があるとき、熱性けいれんの発症が1歳未満のとき、38.9℃以下で熱性けいれんが起きたとき、熱性けいれん再発の確率が高いといわれています。 |
| どのようなとき、病院にかかるべきですか? 救急車を呼んだり、救急外来に連れて行ったりすべきなのは、どんなときですか? | はじめて熱性けいれんが起きたときはすぐに医療機関に受診して下さい。 時計を確認し、けいれんが3分以上続けば、救急車を呼んで下さい。 発作の前後に吐き気、嘔吐、発疹、振戦、異常運動、ふらつきなどの協調運動障害、傾眠傾向、異常興奮、錯乱状態などがみられたり、目つきがおかしかったりしたら、発作がすぐに止まっても、近隣の医療機関になるべく早く相談するか、救急外来を受診して下さい。 |
| どのような検査が行われるのですか? | どのような感染症が原因となって発熱したのか確認するために、のどや鼻の粘膜の拭い液の細菌やウイルスを調べたり、血液や尿の検査をしたりすることがあります。 脳波、頭部CT、腰椎穿刺などの精密検査は必須ではありません。 |
| 熱性けいれんによってどんなことが懸念されるのでしょう? | けいれんにともなう転落、転倒、衝突による外傷。 口に入っていたものによる窒息。 長引く発作による脳損傷。 発熱の原因が細菌性髄膜炎や脳炎のような重症感染症であれば、その後遺症。 発熱を伴わないけいれん(てんかん)への移行。 保護者の方が必要以上に心配され、お子さんの行動、生活を制限してしまうこと。 |
| けいれんを予防する座薬をもらいました。どんなとき役に立つのですか? | お渡ししたダイアップ坐薬を発熱に気づいたときにお尻にいれると、ある程度、けいれんが予防できます。しかし,発熱に気づかないことはよくあるので、ダイアップ坐薬を持っているからといって、絶対にけいれんを予防できるわけではありません。 この座薬を使うと、動きが鈍くなったり,眠気やふらつきがみられたりすることがあるので、注意してください。 |
| 予防接種をやってはいけないのですか? | 熱性けいれんがあっても予防接種はうけてください。予防接種によって生ずる発熱によって熱性けいれんが再発する可能性があることは事実です。しかし、頻度は高くありませんし、予防すべき感染症の発熱によって熱性けいれんが再発する可能性もあります。予防すべき感染症の症状が重いことを考えると予防接種は積極的にうけるべきです。 予防接種によって脳症が起こることはありますが、きわめてまれですし、熱性けいれんの既往があるからといって起こりやすいわけでもありません。 |
熱性けいれんは救急外来でよくみかける疾患です。
突然のひきつけを目の当たりにし、ご家族は大慌てでお子さんを救急外来に連れてこられます。救急車でいらっしゃる方も少なくありません。
しかし、病院に着く頃には、たいてい、ひきつけ(けいれん)は止まっています。けいれんを起こしたご本人はぼんやりしているか、眠ってしまっていることがほとんどです。顔色はまずまずで、呼吸、脈拍も安定していて、多くは、何の処置も要しません。たいてい、「心配いりません」とお話し、家に帰っていただくことになります。
実際、熱性けいれんの多くは、なんの心配もいりません。そして、将来にわたっても、心配する必要がありません。
しかし、高い熱を出し、意識を失い、白目をむいてひきつけた我が子の姿が脳裏に焼きつき、「心配いりません」とはいかない親御さんもいらっしゃいます。うちの子は体が弱く、すぐに病気になってしまう、頭が悪くなるかもしれない、などと必要以上に心配される方が、まれに、いらっしゃいます。
「脆弱児症候群」と呼ばれる状態に陥ってしまう例も報告されています。親御さんの過剰反応によってお子さんの行動にさまざまな異常がみられるようになるのです。そこまでいかなくても、けいれんをおそれて、お子さんの行動を制限してしまう親御さんが、時に、いらっしゃいます。
その一方で、心配のあまり、親御さんが消化不良、食欲不振に陥り、体調不良を訴えられることもあります。けいれんが起こるのではないかと絶えずビクビクし、ちょっとしたお子さんの発熱にも不安になってしまわれる方もみえます。そのために、家庭内がぎくしゃくすることさえあります。
熱性けいれんのイメージの変遷
熱性けいれんを過度に心配される親御さんがみえるのは、無理からぬところがあります。けいれんの症状は激烈ですし、その上、高熱を発しているのですから、どうしても、不吉な印象を受けます。
それに、歴史的にみても、熱性けいれんはあまりいいイメージで見られていないことがありました。
ほんの半世紀前まで、熱性けいれんをたちの悪い疾患とみる考えがあったのです。
その原因のひとつは、熱性けいれんとてんかんの混同でした。 熱性けいれん、とくに、後で述べる複雑型熱性けいれんは、熱によって「仮面がはずれた(unmasked)」てんかんだという主張が医者の間でもなされていました(Livingston (1954))。熱性けいれんは正常な子どもには起こりえないと断言する研究者までいました。
脳炎、細菌性髄膜炎といった中枢神経感染症と混同視されたことも、熱性けいれんのイメージを悪くしました。細菌性髄膜炎や脳炎では発熱に加え、けいれんがみられることが少なくありません。しかし、熱性けいれんと違い、細菌性髄膜炎や脳炎では脳の実質が破壊され、ひどい後遺症を残すことがまれならずみられます。死に至ることもめずらしくありません。そうした疾患と一緒くたにされたため、熱性けいれんに「怖い病気」というイメージが付着したようです。
しかし、当時の診療技術を考えると、それも,無理からぬことでした。ほんの数十年前まで、小さな子の細菌性髄膜炎や脳炎や電解質異常を簡単に診断できる技術がありませんでした。まだ、CTもMRIもない時代です。小さな子供の背中に針を刺し、髄液を採取して髄膜炎を診断するなどということも、一般には行われていませんでした。その上、小さな子には点滴をすることもできず、細菌性髄膜炎が疑われても、血管内に抗生物質を投与するという、今ならどうということもない治療も、当時はできませんでした。
ほんの数十年前まで、脱水で小さな赤ちゃんがバタバタと息を引き取っていくのに、なすすべもなく見ているしかない時代が続いていました。腸にたちの悪い細菌やウイルスが感染し、発熱し,ひどい下痢を繰り返し、なんども吐いて、身体の中の塩分のバランスがむちゃくちゃになって、ひきつけ、亡くなるお子さんが少なからずみえたのです。そうした場合も「熱性けいれん」で死んだとみなされました。
しかし、そうした時代にあっても「熱性けいれん」はそれほど悪性のものではないと考えている医者も少なからずいました。熱でひきつける子の多くは、発作がすぐに止まり、発作の後は比較的元気で、熱が下がってしまえばケロッとしていることを、医者の多くが経験で知っていました。1回や2回熱性けいれんを起こしても、その後の発達に問題を生じない子がほとんどだということもわかっていました。熱性けいれんをおこしながらも,その後、順調に成長し、普通に暮らしている大人がいくらでもいたからです。
そうしたなか、1970年代に決定的に潮流が変わります。それまで暗いイメージをもたらしてきた疾患を除外して熱性けいれんを見直す研究が、欧米を中心に世界中で行われるようになったのです。
その代表が、アメリカ国立衛生研究所(National Institute of Health NIH)が行った周生期共同全国調査National Collaborative Perinatal Project です。55,000人という膨大な数のアメリカ国内の赤ちゃんを、生まれる前から7歳までさまざまな側面から追跡調査した巨大研究です。小児のさまざまな病気について検討がなされましたが、そのひとつが、熱性けいれんを起こした1706人にかんする研究でした。
この研究において重要な出発点となったのは、熱性けいれんの定義です。
「生後3ヶ月から5歳の乳幼児によくみられる、頭蓋内感染などのけいれん誘発性疾患が原因ではない、発熱をともなう発作のことである。無熱性けいれんの既往のある子どもに発熱にともなってけいれんがみられても熱性けいれんとはいわない」
これは、1980年におこなわれたNIH主催の熱性けいれんにかんする会議で合意された熱性けいれんの定義ですが、「熱性けいれんを起こした1706人」というのは、このように定義された熱性けいれんを起こした子どもたちでした。つまり、いままで述べてきた予後不良な疾患を除外し「純粋な」熱性けいれんを対象として追跡調査が行なわれたのです。
この研究のもう一つ大事な点は「普通の子ども」を対象としたことです。追跡調査が行われた55000人は熱性けいれんの1706人を含めてアメリカ全体の子どもを代表するよう人種、性別などに偏りがないよう選ばれていました。一般住民を対象とした地域研究population-based studyだったのです。それ以前の研究は大学病院などの大病院を受診した患者さんを対象に行われることがほとんどでした。そうした病院にやってくる患者さんというのは、どうしても偏りがあります。同じ病気でも重い症状の患者さんが集まってしまいがちです。しかし、病気の本当の姿を知るためには、そうした偏りがない一般の人々を対象とした研究が必要です。このNIHの研究は一般住民を対象とした代表的地域研究でした。
このNIHの研究によって熱性けいれんについてさまざまなことが明らかになりました。
しかし、なんといっても最大の成果は、熱性けいれんの暗いイメージが払拭されたことです。
熱性けいれんを起こしたからといって、必ずしもてんかんの前触れではないし、知能が遅れることもない(熱性けいれんのない兄弟姉妹と比較して差がない)、そのことを、この研究ははっきりと示していました。その後、カナダ、英国、スウェーデン、フィンランド、台湾でも一般住民を対象とした熱性けいれんの研究が行われましたが、大筋において、NIHと同じような結果が得られています。熱性けいれんはその激烈な症状にもかかわらず、あまり心配する必要のない病気であり、成長発達の面でも熱性けいれんのない子と変わりがないという点で、それらの研究は一致していたのです(熱性けいれんの子の方が他の兄弟姉妹に比べ記憶力が優れているという結果を報告をしている研究さえあります)。
こうした地域研究の結果は動物実験によっても確証されています。短時間の熱性けいれんが起きただけの幼弱ラットは、その後、どれだけ観察を続けても、てんかんを起こしやすくなることもありませんし、脳の異常もきたしません。逆に、もともと脳に異常があったラットは短時間の熱性けいれんであっても、その後、てんかん発作を起こしやすくなりますし、熱性けいれんによって神経細胞の異常をきたします。熱性けいれんそのものは無害であることが、ラットにおいても証明されたのです。
以下には、熱性けいれんが、いかにたちのよいものかということを中心に述べたいと思います。
熱性けいれんとは
しかし、その前に、熱性けいれんとは何か,あらましを確認しておきましょう。いままでお話してきたように、熱性けいれんは
「おもに生後満6か月から満60か月までの乳幼児期に起こる、通常は38℃以上の発熱に伴う発作性疾患(けいれん性、非けいれん性を含む)で、髄膜炎などの中枢神経感染症、代謝異常、その他の明らかな発作の原因がみられないもので、てんかんの既往のあるものは除外される(小児神経学会、熱性けいれん診療ガイドライン改定ワーキンググループ(2023)熱性けいれん(熱性発作)診療ガイドライン)」
と定義されています。ここでいう発作とは、脳内の異常電流に起因する発作、すなわち、てんかん発作のことです。てんかん発作が主症状ですから、ある意味、てんかんと同一といってもいい疾患です。ですが、さまざまな理由から、熱性けいれんとてんかんは別ものとして扱われています。
まず、なによりも、熱性けいれんでは必ず熱にともなっててんかん発作が起きます(というか、そのように定義されています)。これに対し、てんかんは「何の誘因もなく」てんかん発作が繰り返される病態をいいます。もちろん、てんかんの患者さんでも、ときとして、発熱にともなっててんかん発作が起きることがあります。風邪をひいて熱がでて、てんかん発作が再発したり、発作がひどくなったりするてんかんの患者さんはときどきみえます。しかし、熱性けいれんと違い、てんかんの患者さんでは熱がないときでも発作が起きます。熱で誘発されることはあっても、通常、てんかん患者さんの発作は「何の誘因もなく」起きます。これに対し、熱性けいれんではてんかん発作にかならず発熱が付随しています。熱もないのにてんかん発作が一度でも起きたら、それは、もはや熱性けいれんではありません。てんかんです。熱という誘発因子がつねにつきまとっているというのが熱性けいれんの絶対的条件です。「無熱性けいれんの既往のある子どもにみられる発熱にともなうけいれん」,すなわち、てんかんのお子さんのけいれんは、はじめから熱性けいれんから除外されます(ちなみに、NIHの定義によるこの「無熱性けいれんの既往のある子どもに発熱にともなってけいれんがみられても、熱性けいれんとはいわない」という除外規定が、上記日本小児神経学会のガイドラインでは「てんかんの既往あるものは除外される」となっています。これは、NIHの定義では、「無熱性けいれん」の中に泣き入りひきつけのような非てんかん性発作が混じってきてしまうことを恐れたためです。このように定義しておかないと、泣き入りひきつけを起こした子が熱でひきつけた場合、「無熱性けいれん」を起こしたのだから熱性けいれんと診断できない、ということになってしまいます。こうした不都合を解消するため日本小児神経学会の定義では「てんかんの既往」と明示されています)。
しかし、これでは、たんなる現象上の定義で、このように定義したからといって、はたして、熱性けいれんを一つの疾患といえるのかと疑問に思われる方もみえるかもしれません。たしかに、熱性けいれんは一つの疾患とはいえない面があります。しかし、熱をともなうけいれんがみられたお子さんたちを集めてみると、いろんな共通点があることも事実です。熱にともなうけいれんは、ほとんどが、乳幼児期に限定され、学童期以降はみられなくなります。さらに、熱性けいれんには家族内発症が認められます。熱性けいれんを起こしたお子さんのご家族には熱性けいれんの既往がある方が多いのです。一つの原因による病気とは断言できないものの、どうやら、熱性けいれんは一括りにして考えてもよさそうです。姿形が似ている病気の集まりを症候群といいますが、熱性けいれんは、その意味では、症候群といっていいでしょう。
ひとつの原因による病気とは言えないと申しましたが、これには2つの意味が含まれています。ひとつは、こうした熱性けいれんの定義にもかかわらず、てんかんの患者さんが紛れ込んでしまうことです。そして、もうひとつは、そうしたてんかんの患者さんを除外しても、熱性けいれんの病因が、症状、経過、予後は似ていても、異なっているということです。
てんかんを除外したといっておきながら,混乱を招くような物言いで、申し訳ないのですが、じつは、熱性けいれんの中にはどうしてもてんかんの子が紛れ込んでしまいます。てんかんをもった子の最初の発作がたまたま発熱によって誘発されたものだったということがあるからです。
その代表例が、ドラベ症候群(重症乳児ミオクロニーてんかん)です。 ドラベ症候群は1歳前の赤ちゃんに発症するきわめて難治なてんかんですが、最初の発作は発熱にともなうけいれんであることが少なくありません。発熱をともなって起きる最初のけいれんは、右半身あるいは左半身優位であったり、いつまでも止まらないけいれん重積であったり、38℃前後と熱がさほど高くなかったりと,普通の熱性けいれんとは様相が異なります。しかし「生後3ヶ月から5歳の乳幼児によくみられる、頭蓋内感染などのけいれん誘発性疾患が原因ではない、発熱をともなう発作」という定義には合致します。ですから、まずは、熱性けいれんの診断がなされます。しかし、2回、3回とけいれんを繰り返すうちに、熱性けいれんではないことが明らかになります。熱もないのに、ほとんど毎日のように、全身けいれん、ミオクロニー発作、複雑部分発作が起こるようになるからです。これは、まぎれもない、てんかんです。その上、「熱性けいれん」を起こすまでは何ともなかったのに、運動の遅れ、知的遅れも目立つようになります。遺伝子解析をすると8割近くで神経細胞の興奮性に関与するナトリウムチャンネルを制御する遺伝子に変異がみつかります。
もう一つ、熱性けいれんをともなう遺伝性てんかん(Genetic epilepsy with febrile seizure plus (GEFS+))という家族性てんかんも、やはり、最初は熱性けいれんと診断されます。6歳過ぎまで頻回に熱を伴うけいれんがみられからです。その後、発熱を伴わないミオクロニー発作、脱力発作、部分発作などがみられるようになって、ようやく、てんかんと診断されます。やはり、細胞膜のナトリウムチャンネルを制御する遺伝子に異常がみられることが多い優生遺伝疾患です(抑制性神経伝達物質GABAの関与するイオンチャンネルの異常がある家系も最近分かってきています)。
熱性けいれんは重症乳児ミオクロニーてんかん、GEFS+のようなてんかんが紛れ込むのを避けることができません。
さらに、こうしたてんかんを除外しても、熱性けいれんはひとつの疾患と言えない面があります。それを端的に示すのが、熱性けいれんの遺伝です。のちほどもう少し詳しく述べますが、熱性けいれんはさまざまな遺伝子異常に関連して発症することがわかっています。
結局、NIHの定義によって姿形は似ているものだけを取り上げても、熱性けいれんの原因はさまざまで、いろんな病気の集まりであるというのが現時点での考え方です。
発作症状:単純型熱性けいれんと複雑型熱性けいれん
熱性けいれんにみられるけいれんは脳の異常電流によって生じる、てんかん発作と考えられています。しかし、てんかん発作にはさまざまな形があります。ところが、熱性けいれんではそのうちのどの発作型が起きているのか、じつは、よく分かっていません。
来院されたお子さんの保護者の方にお聞きすると、大半は、突然、全身を硬直させ、がくがくしたというお答えが返ってきます。昔からのてんかん学の常識から考えると、これは、全般性強直間代発作ということになります。事実、昔から、そのことを前提として熱性けいれんについての検討がなされてきました。
ところが、熱性けいれんの発作は全般性強直間代発作だという確たる証拠はありません。
てんかん発作の診断には発作時脳波記録が一番確実ですが、報告数がきわめて限られます(メモ1)。国内外で三つぐらいしか報告されていません。この三つの報告いずれも、見た目の発作症状は強直間代発作なのに脳波では強直間代発作の前に部分発作起始を疑わせる所見が確認されています。もちろん、たった3例だけで、これが熱性けいれんの発作時脳波像と断定することはできません。熱性けいれんの3分の2は再発することがありませんし、一回の発熱時に発作を繰り返すことも滅多にありません。そんな中で発作時脳波が記録できたのはかなり特殊な例だった可能性もあります。とりあえずは、例外的な脳波所見と見なしておいたほうがいいかもしれません。
| メモ1 熱性けいれんの発作時脳波報告例 まず、私の先輩の前原先生による1歳10か月の女の子の報告です(前原光夫(1988) 熱性けいれんの発作時脳波 臨床脳波 30:478-80)。発熱にともない「呼びかけに対する反応が鈍くなり、ボーッとした表情になり、動作も緩慢になった」ということで、複雑部分発作を疑われ、すぐさま脳波が記録されました。しかし、前頭部の波が遅くなってはいましたが、脳波上、てんかん放電は認めませんでした。熱に伴うもうろう状態があったのかもしれないと疑われながら脳波記録が続行されたところ、脳波記録開始後20分たったところで、突然、キャーという叫声とともに、眼球が上転、体幹、四肢を強直させ、続いて、間代する発作がみられました。発作は2分続きました。脳波上には、左側頭部―後側頭部に棘波が目立つ、左右バラバラな不規則な棘徐波がみられました。そして、そのあと、高振幅律動性棘波がしばらく続きました。その後、徐波が混じるようになり、棘徐波に移行しています。高振幅律動性棘波がみられたあとは、全般性強直間代発作の典型的な脳波で、ビデオが撮像されていないので正確に症状と脳波変化を詳細に比較することはできませんでしたが、高振幅律動性棘波に対応して「体幹、四肢を強直させ」、棘徐波のとき「間代させる発作」がみられたのだろうと推定されます。ここで問題なのは高振幅律動性棘波が出現する前です。「左側頭部―後側頭部に棘波が目立つ、左右バラバラな不規則な棘徐波」というのは全般性強直間代性発作では、普通、みられません。症状は不明ですが、おそらくは、部分発作を示している脳波像で、脳波検査前の一回目の発作のときは強直間代発作に移行せずにこの部分発作が続き、複雑部分発作の症状を示したのだろうと想像されます。ちなみに、この女の子は、その後、3歳5か月まで発熱時のけいれんはなく、発達も正常でした。 もう一人は生後11か月のフランスの男児です(Hamelin S, Vercueil L (2014) A simple febrile seizure with focal onset Epileptic Disord 16: 112-5)。母親が特発性全般てんかんの診断でバルプロ酸を服用していました。この男の子は生後9か月に2回熱性けいれんを起こしました。単純型熱性けいれんだったということですから、部分発作の要素のない、普通の全身けいれんが熱に伴ってみられていたと思われます。ビデオ-脳波同時記録を開始時、熱はありませんでしたが、記録開始後に中耳炎によるとみられる発熱がみられるようになり、体温は38.8度にまで達しました。男の子は電極を装着しているうちに寝入ってしまいましたが、その数分後、脳波上、不規則徐波が出現し、男の子は目を開け、泣き出しました。すると、右中心側頭部に10-15Hzの律動波が出現、やがて、この律動波は左に広がり、やがて、両側に律動性棘波が出現、その後、棘徐波に移行しています。有名な Epileptic syndromes in infancy, childhood and adolescenceという本の第4版(Roger et al., 2005) に単純型熱性けいれんの発作時脳波として報告された症例ですが、脳波上、部分起始から両側性発作に移行しているので、全般性発作とは言えないと報告者はコメントしています。その後9年間の経過観察中、熱性けいれんも、てんかん発作も起きておらず、正常に発達しているとのことです。 最後は、2歳8か月の日本人の男児です(Taku T et al (1991) Ictal EEG in febrile convulsions: a case report. Brain Dev 13:207)。学会発表の要約文で実際の脳波が提示されていないので詳しいことはわかりませんが、脳波上、右頭頂後頭部に鋭波がみられ、ついで、全般性の不規則鋭波に移行、全般性多棘波、全般性棘徐波がみられた後、脳波活動が抑圧されたと書かれています。発作は全般性強直間代発作で脳波も全般性強直間代発作にみられるものと同じだと発表者は主張していますが、全般性多棘波、全般性棘徐波は強直間代発作の発作時脳波でいいとしても、右頭頂後頭部の鋭波、全般性の不規則鋭波は全般性強直間代発作にみられるものでなく、やはり、部分発作の全般化が疑われます。この男の子も6歳まで問題なく正常に発達しているようです。 |
しかし、このような、部分発作が先行する2次性全般化強直間代発作は乳幼児期のてんかん発作の特徴といえるものです。たとえば、熱性けいれんの好発する乳幼児期のてんかん、良性乳児けいれん(自然終息性家族性非家族性乳児てんかん)です。元々、この良性乳児けいれんの発作も全般性強直間代発作と考えられていたのですが、実際には、部分発作のことが多く、全身けいれんの様にみえてもビデオ・脳波同時記録(発作が群発する傾向があるので、かなりの記録が残されています)では部分発作起始であることがわかっています(Watanabe K, et al (1993) Benign partial epilepsy with secondarily generalized seizures in infancy. Epilepsia 34:635-8)。
乳児期のてんかんといえば、もう一つ、良性乳児てんかんよりは数は少ないですが、重症乳児ミオクロニーてんかん(ドラベ症候群)があります。この重症ミオクロニーてんかんにみられる全身けいれんも、しばしば左右差がみられますし、ビデオ-脳波同時記録では何らかの脳波上の焦点性がみられます。少なくとも、典型的な全般性強直間代発作とはいえません。
乳児期を過ぎて幼児期にけいれん発作を起こすてんかんで多いのは中心側頭部棘波を示す特発性てんかんですが、やはり、実際の発作はシルビウス発作という部分発作とその全般化発作です。似たものに、後頭葉から始まる特発性てんかんがありますが、やはり、後頭部から始まる発作が主体で、全般性強直発作ではありません。つまり、熱性けいれんの好発時期である乳児期、幼児期において、発作時脳波で全般性強直間代発作があると証明されているてんかんはないのです。
発作時脳波のことは横に置いておいて、では、症状だけでみるとどうかというと、じつは、これにかんしても、熱性けいれんにおいては部分発作が先行しているのではないかという報告が少なくありません。全身をけいれんさせる前に、表情が変わったり、一点を見つめたり、動作が停止したり、目がどちらかに寄ったりしている例が少なくないのです。そうした部分発作に気づかれずに全身けいれんを起こしたと保護者の方がおっしゃることもあるのですが、その全身けいれんというのが、全身を硬くさせただけということが少なくありません。全般性強直間代発作のうちの、間代、すなわち、しばらく全身をガクガクさせる動きをみてみえないというのです。もしこれが本当なら、全身けいれんは強直間代発作ではなく、全身の強直を伴う部分発作の可能性が高くなります。
ということで、聞き取り調査の結果からも、どうやら、熱性けいれんでは全般性強直間代発作ではなく部分発作、もしくは、部分発作の2次性全般化発作が大半を占めている気配が濃厚です。発作時脳波が記録された症例に見られたような報告は、けっして、例外ではないようなのです。
ここまで聞いてこられて、発作についてのそんな些末な議論などどうでもいいじゃないか、と感じられる方もいらっしゃるかもしれません。たしかにそうです。しかし、熱性けいれんにかんしては、そうもいっていられない事情があります。
熱性けいれんは、歴史的に、単純型熱性けいれんと複雑型熱性けいれんの二つに区分けされてきました。複雑型熱性けいれんというのは
- 複雑部分発作を含む焦点性発作(部分発作)
- 発作が15分以上持続遷延
- 1発熱時に2回以上の発作の反復
のいずれかが認められる熱性けいれんのことをいいます。そして、以上の3つのいずれもみられないものを単純型熱性けいれんと呼んできました。
この区分けを言いだしたのは先程述べたNIHの研究プロジェクトです。熱性けいれんを二つに分け、複雑型熱性けいれんがてんかん発症につながる可能性が単純型熱性けいれんに比べて高いことを示したのです。NIHのこの研究はその後の熱性けいれんの研究に大きな影響を及ぼし、熱性けいれん後のてんかん発症を予測するにあたって、この単純型と複雑型という区分はその後の研究にも引き継がれました。そして、通常は詳細な発作症状を調べることのない大規模地域研究などでは複雑型熱性けいれんの頻度がせいぜい10%程度とされてきました。
しかし、発作型を詳しく検討することによって、こうした研究の積み重ねが一挙に崩れてしまいます。
いうまでもありませんが、上の条件の1、「複雑部分発作を含む焦点性発作(部分発作)」という条件が問題となるのです。先程の議論からすると、この条件の下では熱性けいれんのほとんどは複雑型熱性けいれんということになってしまいます。単純型、複雑型という区分そのものが意味のないものになってしまうのです。こうした不都合があるために、複雑型熱性けいれんの条件から発作型ははずすべきだと意見が出てきています。さらに、発作の長さも当てにならないのだから(初めて見るわが子のひきつけに動揺して発作時間を長く(たとえば1分を10分に)申し立てる家族の方がみえますから)、そもそも、熱性けいれんを単純型と複雑型に分けるべきではないという意見もあります。しかし、この区分けには長い歴史があり、それを用いた数多くの重要な研究が積み重なっています。熱性けいれんを語る場合、いまさらそれらの成果をすべてご破算にはできません。熱性けいれんについて話そうとすると、とりあえずは、触れざるをえないのです。事実、本稿でも、これ以降、時々この単純型、複雑型という区分けが出てきます。その場合、単純型熱性けいれんは先行症状の有無はともかくも、発作の主体は「左右対称性の全身けいれん」の熱性けいれんぐらいに考えていただければと思います。
熱性けいれんには3つの要素が関与します。
熱、体質、そして、年齢です。
この3つに注目すると、熱性けいれんは理解しやすくなります。
体温
体温は、時間帯、食事、測定部位など、さまざまな要因で変動します。 活発に動く昼間の方が体温は高いですし、肉を食べると体温が0.3度ぐらい上がるといわれています。また、腋の下の温度(腋下温)は口腔内の温度、肛門内の温度(直腸温)に比べ低めです。 こうした不確定要素があるからでしょう、何度以上の体温でけいれんを起こせば熱性けいれんといえるか、きちんと書かれていない熱性けいれんの定義もあります。しかし、ここでは38.3度以上を発熱とみなしているShinnarたちの定義に従うことにします。しかし、この値は直腸温、口腔温測定が一般家庭の間でも広まっている欧米での定義ですので、日本で一般的な腋下温であれば、体温が38℃以上ならば「熱がある」と考えていただいていいだろうと思います。ということで、日本小児神経学会の熱性けいれん診療ガイドラインも熱性けいれんを「通常は38度以上の発熱にともなう発作性(けいれん性、非けいれん性を含む)疾患」と定義しています。
ただし、発作が起きたときの体温が38℃以上でなければ熱性けいれんとはいえない、というわけではありません。発作が起きる前後、いずれかの時点で,体温が38度以上あればいいということになっています。発作が起こっている最中、熱がさほど高くなくてもかまいません。だいいち、慌てていて、よほど高い熱でないかぎり、熱に気づかないことがあります。発作後、数時間して熱に気づかれることは、熱性けいれんではよくあることです。定義において「発熱に起因する発作」といった熱と発作を直接結びつける表現ではなく「発熱にともなう発作」と、やや曖昧な表現になっているのはそのせいです。
発熱したら、すぐに、発作を起こすというわけでもありません。発熱後1時間以内にけいれんが起こるのはせいぜい2割程度です。24時間以上たってからけいれんを起こすことも2割程度みられます。あとの6割は、発熱後1時間から24時間にけいれんが起きます。
熱をだす病気というと、日本では夏かぜとインフルエンザなどの冬のかぜが思い浮かびます。実際、日本で熱性けいれんが起こりやすいのは夏と冬です。しかし、熱性けいれんのこの季節性は万国共通ではありません。たとえば、スウェーデンでは夏休暇が終わり、乳幼児が託児所や保育園に戻ってくる秋に熱性けいれんが多いようです(ちなみに、託児所や保育園に通っているお子さんは感染症にかかりやすいため、熱性けいれんにもなりやすいことが知られています。ただし,人口密度の高い大都市では、そういったところに通っていなくても感染症にかかりやすいので、託児所や保育園に通っているお子さんと通っていないお子さんの間で熱性けいれんの頻度にはっきりした違いはみられません)。
発熱を起こす疾患別でみると、いわゆる胃腸カゼ(胃腸炎)では熱性けいれんが起こりにくいことがわかっています。理由はわかっていません。一方、突発性発疹症(突発疹)は熱性けいれんを引き起こす感染症として有名です。初発熱性けいれんの約4分の1は突発疹の発熱が原因です。とくに、2歳以下では、初発熱性けいれんの3分の1で突発疹の発熱が引き金になっています。突発疹の原因となるヘルペス族ウイルス、HHV-6とHHV-7は神経細胞に親和性があります。そのことが、熱性けいれんを起こしやすいことと何か関係があるのかもしれません(赤ちゃんが最初に高熱を出す疾患が突発疹だからという説明もなされています)。突発疹の原因となるこれらヘルペスウイルスは、15分以上続く遷延性熱性けいれんの主要原因でもあります。
このように、発熱をきたす疾患によって熱性けいれんの起こりやすさは違います。このことは、熱そのものはけいれんの直接の原因ではない可能性を示唆しているようにもみえます。実際、先ほど述べたように、けいれんの直前にはほとんど発熱していなかったという熱性けいれんの例が結構あります。
しかし、では、発熱以外の何がけいれんの誘因になっているのかというと、まだ、よくわかっていません。
ただ、研究者が目星をつけているものが、いくつか、あります。
そのひとつが、インターロイキンです。 インターロイキンは白血球が産生するタンパク質で、外敵から身を守る免疫反応において、さまざまな手助けをしています。20種類以上のインターロイキンが知られていますが、熱性けいれんとの関連が注目されているのは、インターロイキン‐1β(IL-1β)という物質です。細菌感染やウイルス感染のときに白血球から放出される炎症性タンパク質で、微生物を体内から駆逐するためのさまざまな機能を発揮します。そうした機能のうちでも、脳の中央に位置する視床下部の体温中枢を刺激し、体温を高める作用がなんといっても重要です。発熱を誘発することから内因性発熱物質とも呼ばれています。ヒトは主としてIL-1βを介して発熱することがわかっています。前に述べましたように、熱性けいれんでは、けいれん時の体温ではなく、発熱期間中の最高体温がけいれんを起こすかどうかの鍵を握っています。このことは、発熱をきたすIL-1βの量が多ければ多いほどけいれんが起きやすいことを暗示しているようにみえるのです。一方で、IL-1βは、直接、神経の興奮性も高めます。高濃度のIL-1βを動物の脳に投与するとけいれんを起こすことが知られていますし、IL-1βの受容体を邪魔する物質はけいれんを抑えることがわかっています。その上、熱性けいれんを起こしたお子さんの髄液内には高濃度のIL-1βが検出されています。以上のようなことから、IL-1βが熱性けいれんの発症に何らかの形で関与しているらしいことはおわかりいただけるかと思います。しかし、では、IL-1βが熱性けいれんの原因と言い切れるかというと、そういうわけでもありません。まだまだ、解決すべき課題がたくさん残されています。
一方、熱性けいれんのお子さんの一部で、画像上、急性脳症と見まがう所見がみられる例があることが報告されています。左右の脳を線維連絡する脳梁といわれる構造物が脳の真ん中にありますが、熱性けいれんのお子さんでMRIをとると、この脳梁が水っぽくなっていることがあるのです。これは軽い急性脳症や熱性譫妄のお子さんにもみられる所見ですが、そうした疾患で、なぜ、脳梁が水っぽくなるのか、理由はわかっていません。また、脳梁が水っぽくなる熱性けいれんと、そうでない熱性けいれんが違うものなのかどうかも、今のところ、わかっていません。しかし、発熱が、何らかの変化を脳にもたらし、それが、けいれんに結びついているらしいことは、ぼんやりとではありますが、このMRI所見からも想像できます。
このように、熱性けいれんの発生機序についてはいろいろな事が少しずつわかってきています。しかし、謎も多く、完全に解明されるのは、まだまだ、先のことになりそうです。
次に、体質、あるいは、遺伝です。
熱性けいれんに遺伝が関与していることは、熱性けいれんを起こした子に熱性けいれんの既往のある家族が多いことからもわかります。熱性けいれんの子の両親が熱性けいれんの既往がある頻度は10~15%、兄弟姉妹の熱性けいれん既往は20%前後で、一般の熱性けいれん罹患率に比べ高いことがわかっています。しかも、同じ兄弟姉妹でも遺伝構造が似ている一卵性双生児では、二人とも熱性けいれんに罹患する確率がさらに高く、56%です。一方、二卵性双生児の罹患率は普通の兄弟姉妹の場合とあまり変わりません。さらに、兄弟姉妹が熱性けいれんを発症した場合、発症年齢、熱性けいれん時最高体温など熱性けいれんの臨床的特徴が双子の同胞例では似かよっていることもわかっています。
こうしたことから、遺伝要因が熱性けいれん発症にかかわっていることは間違いなさそうです。
しかし、では、熱性けいれんがメンデルの法則につき従うような遺伝をするのかというと、そういうわけではありません。現在までのところ、熱性けいれんを引き起こす唯一無二の遺伝子はみつかっていません。単一遺伝子ではなく、さまざまな遺伝子の変異が熱性けいれんと関連しているらしいことがわかっているだけです。たとえば、連鎖解析という手法によって2番、3番、5番、8番、18番、19番染色体の遺伝子異常が熱性けいれん発症にかかわっていることが判明しています。つまり、いろいろな部位の遺伝子異常が最終的に症状として(表現型として)熱性けいれんという形をとっているらしいのです。しかし、そうしたいろいろな部位の遺伝子異常がどのようにして熱性けいれんという症状に結びつくのかは、まだ、わかっていません。遺伝子異常から熱性けいれんに至る道筋は謎のまま残されています。
しかし、いずれにしても、以上のことから、前に述べましたように、熱性けいれんというのは、たったひとつの原因によって起こる疾患ではないことだけはわかります。熱を伴う発作で始まる「隠れてんかん」を除いても、さまざまな原因が熱性けいれんを引き起こします。前に述べたように熱性けいれんは、姿形は似ているものの、さまざまな原因による病気の集まりなのです。
熱性けいれんは単純なメンデルの法則に従うような遺伝形式をとらないと申しましたが、症状の出現が、熱という、ある種の環境要因に依存していることも、分かりにくくしている原因の一つです。
熱性けいれんは環境因子(発熱)と体質の相互作用によって発症する疾患です。 体質と環境が相互に影響しあって発症する疾患としては高血圧(塩分のとりすぎ)、糖尿病(過食、もしくは、運動不足による肥満)などさまざまなものがあります。これらは、いずれも遺伝子(体質)の関与がいわれているにもかかわらずメンデルの法則通りの発症形式をとりません。環境条件によっては発症しないことがありうるからです。熱性けいれんもそのひとつで、環境因子(熱)によっては発症しないことがありえます。
さらに、熱性けいれんの遺伝子(体質)をもつお子さんが高熱をだすと必ず熱性けいれんを起こすというわけでもありません。同じ発熱であっても、発熱をきたす病気によって、熱性けいれんの起こりやすさが異なるからです。前に述べましたように、突発疹は熱性けいれんを起こしやすく、胃腸炎の発熱では熱性けいれんはあまり起きません。
また、発熱する機会が少ない場合も、当然、熱性けいれんを起こす可能性は下がります。逆に、託児所や保育園に通っている子は熱性けいれんを起こす可能性が高くなります。このように、熱性けいれんの素因をもっていても、幼児期に罹患する感染症の種類や頻度によっては熱性けいれんを起こさないこともありえます。逆に、熱性けいれん体質がさほど強くなくても、感染症の種類によっては熱性けいれんを起こしますし、長いけいれんを起こしてしまうこともありえます。
最後に年齢です。 熱性けいれんは年齢依存性の疾患です。
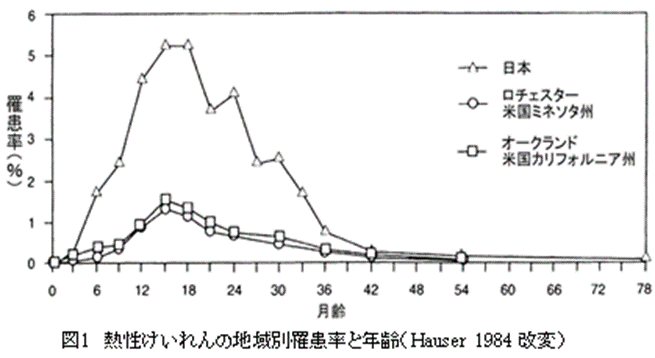
図1をみていただければ一目瞭然ですが、だいたい、生後6か月から3歳、このあたりが、熱性けいれんの好発年齢です。そして、初発年齢のピークは1歳半前後です。5歳をすぎると熱性けいれんはほとんどみられなくなります。成人してから熱によるひきつけを繰り返す方はいません。熱性けいれんは、乳幼児期に一時的にあらわれ、成長とともに消えていきます。つまり、熱性けいれんは特定の発達段階の脳にあらわれる疾患群といっていいでしょう。
ちなみに、日本小児神経学会熱性けいれん診療ガイドラインでは熱性けいれんを「おもに生後6~60か月の乳幼児期に起こる」と定義していますが、5歳を過ぎてから、はじめて、熱性けいれんが起きる子がまったくいないわけではありません。しかし、まれです。そして、そうした子たちも10歳までに、発熱にともなうけいれんを起こさなくなります。5歳過ぎに初発する熱性けいれんは例外的なので、たちが悪いのではと心配される保護者の方もみえますが、発作予後、知的予後も含め、もっと小さい頃に初発する熱性けいれんとほとんど変わらないことがわかっています。ですから、5歳過ぎの発症でも、5歳までに発症した熱性けいれんと同じように扱ってもいいと考えられています。
微量元素
炭水化物の構成要素の炭素、あるいは、タンパク質を形作る窒素のように大量に体内に存在する元素とは対照的に、生命維持に不可欠なのに体内含有量が少ない元素を微量元素といいます。どのぐらいを微量というかですが、目安となるのが鉄です。鉄の含有量は成人男性で3000~5000mgです。そこで、体内含有量がだいたい50000mg以下が微量ということになっています。鉄以外に、亜鉛、セレン、銅、マンガン、ヨウ素、モリブデン、クロム、コバルトが微量元素で、大体が金属イオンです。最近、この微量元素の一部と熱性けいれんの関係が報告されるようになってきています。
まずは、亜鉛です。血中亜鉛濃度、髄液中亜鉛濃度の低値が熱性けいれんの起こりやすさと関連していることが報告されています。なぜ亜鉛に目がつけられたかと言いますと、亜鉛イオンが神経接合部であるシナプス内顆粒に含まれていて、神経細胞の活性化に伴って放出されているからです。そして、動物実験では脳の亜鉛イオン濃度が低いとてんかん発作が起こりやすいことが証明されています。ただし、今のところ、たとえば、熱性けいれんを起こして亜鉛濃度が低めだった子に亜鉛濃度を高くするような(レバー、卵、チーズ、納豆、えんどう豆、ピーナッツ、アーモンド、牡蠣、あわび、かになどの亜鉛が多い食品と食べたり、亜鉛サプリを呑んだりして)対策を施したら、熱性けいれんの再発率が下がったというような報告はありません。
次に、鉄です。鉄に関しては、昔から、泣き入りひきつけとの関連がよく言われていまして、鉄剤を服用すると、明らかな鉄欠乏性貧血がない子でも泣き入りひきつけの頻度が減ることが知られています。鉄欠乏によってなぜ泣き入りひきつけが起こりやすくなるのか、正確には分かっていません。鉄は神経伝達物質としても働くアミン(セロトニン,ドーパミン,ノルアドレナリン)の合成に必要な微量金属ですから、それが何か関係しているのかもしれません。あるいは、鉄欠乏による貧血で体調不良で過敏状態になっているかもしれません。
このように、この泣き入りひきつけに関連する鉄ですが、最近、熱性けいれんにも関係しているのではないかといわれるようになってきました。熱性けいれんを起こした子はけいれんを起こさない子に比べて鉄欠乏性貧血の頻度が高いことがわかってきているのです。しかし、亜鉛と同じように、鉄剤を服用して鉄欠乏傾向を改善させれば熱性けいれんを改善できるかどうかについての検討は、今のところ、なされていません。ただ、鉄欠乏性貧血は全身への酸素運搬効率を下げるわけですから、熱性けいれんのありなしとは無関係にきちんと対応しておいた方がいいでしょう。
もう一つ、セレンの低値も熱性けいれんの子に多いと言われています。しかし、これも、なぜなのか分かっていません。セレンは活性酸素から生体を守るのに大事な物質ですが、それが、熱性けいれんとどのように結びつくのか、うまく説明できていません。それに、やはり、セレン摂取を増やすことが熱性けいれん予防につながるかどうかも分かっていません。セレンは過量摂取による中毒もありますから、取り過ぎにも注意が必要です。
過呼吸
熱がでると息が荒くなって、過換気状態になります。すると、二酸化炭素が必要以上に呼気から吐き出され、血液の炭酸が抜き取られて、身体がアルカリ性に傾きます。呼吸性アルカローシスと呼ばれる状態です。脳の神経細胞はアルカリ性に傾くと興奮性が高まりますから、けいれんが起きやすくなることが予想されます。このことはラットなどの動物実験で確認されていますし、てんかんの人が熱で発作頻度が増えるのもこの道筋を通ってかもしれないと指摘する人もいます。もしそうなら、熱性けいれん発生にもこのことが関係しているかもしれません。事実、胃腸炎で発熱した子に比べ熱性けいれんを起こした子は血液の二酸化炭素濃度が低く、したがって、アルカリ性に傾いていたという報告があります。ただ、これは発作のあとの値で比較しているので、単純に熱でアルカリ性に傾いたので熱性けいれんが起きたと断言していいかどうかは分かりません。
頻度
図1をご覧になってびっくりされた方もいらっしゃるかもしれませんから、熱性けいれんの発生頻度について、ここで、簡単に触れておきます。 熱性けいれんは小児に痙攣(てんかん発作)をもたらす原因としては飛び抜けて多い疾患で、2%から5%のお子さんにみられるとされています。つまり、100人に2人から5人にみられるということになります。いかにありふれた病気かわかります。しかし、この100人に2~5人という数字は世界の国々の中の平均的値で、国によって熱性けいれんの罹患率はかなりの差があります。図1でおわかりだと思いますが、日本は熱性けいれんの罹患率が飛び抜けて高く、8.8%です。1984年に報告された図1ではそれが反映されています。これによれば、日本の子どもの一割近くが一度は熱性けいれんを経験するということになります。熱性けいれんの遺伝的素因の高い人が日本には多いということなのかもしれません。しかし、日本人の熱性けいれん罹患率がなぜ高いのか、その本当の理由は、よくわかっていません。それに、この8.8%という頻度は保健所の乳児検診、小学校の児童検診の結果を基にして算出されたものです。その後行われた岡山県玉野市における疫学調査では3.4%という結果が報告されています。世界の平均とほとんど変わらない頻度です。どちらが、日本の正しい有病率を反映しているのか、その後、大規模調査が行われていないので、議論の決着はついていません。
ついでながら、日本よりさらに高い熱性けいれん罹患率が報告されている地域があります。
グアムです。グアム島では100人中14人が熱性けいれんを経験すると推定されています。
逆に、熱性けいれんがかなり少ない国もあります。たとえば、イタリア、メキシコの熱性けいれん罹患率は1%台です。
熱性けいれんがみられた子の保護者の方が一番心配されるのは、熱がでると、また、同じことが起きるのではないか、うちの子が、また、叫び声を上げ、すごい形相になって、ひきつけるのではないか、ということです。たしかに、何度も熱によるけいれんを繰り返す子がいます。しかし、その頻度はそれほど高くありません。熱性けいれんを起こした子のうち、熱をだして、再度、発作をおこすのは、3分の1です。残りの3分の2の子は、二度と熱性けいれんを起こすことはありません。3回目を起こす確率はさらに低く、約1割です。万が一、2回目の熱性けいれんを起こしても、やはり、3人に2人はそれ以上熱性けいれんを起こすことはありません。
再発は最初の熱性けいれんから2年以内がほとんどです。再発のほとんど(9割)は初発発作から2年以内に起きます。そして、再発の3分の2は1年以内です。2年を過ぎると、再発の可能性はかなり下がります。
再発するかどうか、1人1人のお子さんについて正確に予測することは、残念ながら、できません。
しかし、ある程度の目安はわかっています。
まず、当たり前の話ですが、発熱回数が多いほど、再発の可能性は高くなります。これに対処するには、感染機会を減らせば良いわけですが、そのためには悩ましい選択を迫られることになります。感染機会を減らすとなると、保育園や幼稚園に行かない、公園にも遊びに行かなければいいわけです。しかし、熱性けいれんの再発を恐れて子どもの発達に必要な子ども同士の交流の場を狭めるのは、本末転倒です。どんな疾患についても言えることですが、治療の最終目標は、病気の症状を消し去ることだけではありません。病気の症状によって、通常の生活が阻害されることを避けることも含まれます。それを考えれば、子どもにとって一番優先されるべき発育、発達の邪魔をすることなど、治療の名に値しません。
ただし、生活を阻害せずにお子さんの発熱の機会を減らす方法が一つあります。予防接種です。最後のところで、詳しく述べますが、予防接種によって熱がでる可能性はあるものの、予防接種によって発病が阻止される麻疹や水ぼうそうなどによる発熱の方が圧倒的に熱性けいれんを誘発する危険性が高いことが知られています。ですから、熱性けいれんの子は積極的に予防接種をすることが勧められます。
発熱機会以外で再発が起こりやすくなる要因としては1)小さい頃(特に1歳未満)に発症していること、2)ご両親が熱性けいれん起こしたことがあること、3)熱性けいれん時の最高体温が低い(≦39℃)こと、そして、4)発熱からけいれんまでの時間が短い(一時間未満)こと、などが挙げられます。
とくに、熱性けいれんの若年発症は熱性けいれん再発と強い相関があります。たとえば、1歳半以前に最初の熱性けいれんがみられたお子さんは、1歳半以降に初回熱性けいれんがみられたお子さんに比べ、再発率が約2倍です。小さい頃に熱性けいれんを起こしたお子さんの再発率が高いのは、ある意味、当然です。もう一度、図1をご覧下さい。熱性けいれんは1歳半を中心に、生後半年から3歳までにその大半が起きる疾患です。小さい頃に熱性けいれんが起きると、その熱性けいれん危険年齢帯を数年にわたってくぐり抜けていかなければなりません。当然、年齢がある程度いってから熱性けいれんが起きるお子さんに比べ、熱性けいれんをもう一度起こす機会は多くなります。
両親など家族に熱性けいれんの既往があるお子さんの熱性けいれん再発率も、家族に熱性けいれんの既往のない子に比べ、1.5倍から2倍高いことが知られています。熱性けいれんの体質が強い子は何度も熱性けいれんを起こしやすいということなのでしょう。ただし、熱性けいれんの再発に関係するのは熱性けいれんの家族歴であって、てんかんの家族歴ではありません。てんかんの家族歴は熱性けいれん後のてんかんの発症とは関連しますが、熱性けいれんの再発との関連はあまりありません。
熱性けいれん時、最高体温が低い(≦38.3℃)ことも再発の危険因子といわれています。熱に対するけいれん感受性が高いと再発しやすいということなのかもしれません。いろいろな報告がなされていますが、最高体温が高い群に比べて低い群では再発が2-3倍高いと推定されています。
発熱からけいれんまでの時間が短い子に再発率が高いというのは、最初に述べた発熱機会との類推から納得できます。同じ発熱と言っても、数時間でおさまるものから24時間以上続くものまであります。数時間でおさまる発熱だと、発熱から半日以上たってから発作が起きる子では当然発作が起きる確率は低いでしょう。これに反し、発熱後1時間以内に起きる子では発熱期間が短くても発作が起きてしまうでしょう。
熱性けいれん再発の可能性は以上述べた危険因子が多いほど高まります。危険因子が2個、3個、4個の場合、初発熱性けいれんから2年以内の熱性けいれん再発率は、それぞれ、30%、60%、70%といわれています。逆にこうした危険因子がないお子さんの熱性けいれんの再発率は15%前後です。
けいれんが長く続く遷延性熱性けいれんの場合も、再発率が高いように思われがちですが、幸いなことに、遷延性熱性けいれんがあったからといって、必ずしも、再発率は高くありません。ただし、万が一再発すると、再び、発作が遷延する傾向があります。初回熱性けいれんが遷延した場合、再発時のけいれんも遷延する危険性は2~4倍です。
ちなみに、熱性けいれん発症以前の精神運動発達異常、複雑型熱性けいれんの有無、民族、性別は熱性けいれん再発との関連がないといわれています。
てんかんになりやすい?
熱性けいれんとてんかんは別物だと申しました。しかし、それでも、不安に思われる方がみえるかもしれません。熱をともなうとはいえ、現実にてんかん発作を起こしているわけですから、てんかん発作を起こしやすい体質をもっているのではないか、という疑問は、どうしても、拭いきれません。
熱性けいれんの既往のあるお子さんがてんかんを発症する頻度は2-7%です。頻度に幅があるのは報告によって観察期間が異なるためで、25歳まで経過を追っていったら7%がてんかんに移行したという報告もあって、これが最長の観察期間です。小児全体のてんかん発症率は0.5-1%と言われていますから、熱性けいれんの子のてんかん発症率はたしかに高率です。しかし、逆に考えれば、熱性けいれんの子の9割以上はてんかんを発症することはないわけです。熱性けいれんになったからといって、大半のお子さんでは、てんかんの発症に結びつくわけではないのです。
しかし、たしかに、一部のお子さんはてんかんを発症します。ただ、その場合でも、熱性けいれんが「悪化して」てんかんになるわけではありません。
てんかんになるかどうかは、熱性けいれんの「形態」によってある程度決まるといわれてきました。熱性けいれんを起こした子がてんかんを発症する頻度は2-7%であるのに複雑型熱性けいれんの子のてんかん発症頻度は10~20%ということが定説になってきました。
ただし、熱性けいれんに続発するてんかんの病型はさまざまです。熱性けいれんの既往があるお子さんに特徴的なてんかんというものはありません。熱性けいれんの経験がないお子さんのてんかんと大して変わりません。
逆にみますと、小児期発症てんかんを有するお子さんの10%から20%に熱性けいれんの既往が認められます。しかし、やはり、そのてんかんには良性ローランドてんかんや小児欠神発作などさまざまなてんかん類型が含まれ,特定のてんかん症候群が飛び抜けて多いということはありません。つまり、一口にてんかんといっても、実にさまざまな形のてんかんと熱性けいれんは結びついているのです。
さらに言いますと、熱性けいれんに続発するてんかんの多くは、特発性てんかん、すなわち、体質や遺伝が関連するてんかんです。このことは、熱性けいれんからてんかんに移行する例のほとんどでは、熱性けいれんはてんかんの原因ではなく、起点にすぎないことを暗示しています。その代表例が、先に述べた熱性けいれんをともなう遺伝性てんかん(Genetic epilepsy with febrile seizure plus : GEFS+)です。細胞膜のナトリウムチャンネルに関与する遺伝子に異常がみられることのある優生遺伝疾患で、6歳過ぎまで頻回に熱性けいれんが起こり、その後、部分発作、ミオクロニー発作、脱力ミオクロニー発作などがみられるようになって、てんかんと診断されます。
このGEFS+のように、熱性けいれん後のてんかんの大半は熱性けいれんが「悪化して」てんかんになるのではなく、むしろ、てんかんを発症するようなお子さんが、小さい頃、たまたま、熱によるけいれんを起こしたと考えてよさそうなのです(ただし、きわめてまれな例外があります。それが、後で述べる、片側けいれん-片側麻痺-てんかん症候群にみられるてんかん、それに、海馬硬化による側頭葉てんかんです)。
ひとりひとりで、熱性けいれんの後にてんかんを発症するかどうか、きちんと言い当てることはできません。しかし、どういう子がてんかんになりやすいかは、ある程度、わかっています。
まずは、ご家族にてんかんの既往がある子です。熱性けいれんに続発するてんかんに素因が関与していることが、このことからもわかります。
さらに、症状の項で述べたように、複雑型熱性けいれんの子もてんかんに移行しやすいことがわかっています。複雑型熱性けいれんの子のてんかん発症率は10~20%で、とくに、複雑型熱性けいれんの3要素をすべてもっている子が成人するまでにてんかんを発症する可能性は50%といわれています。ただし、そのような子は熱性けいれんの1%を占めるにすぎません。
また、熱性けいれんを起こす前から発達に異常がみられていた子、とくに、生下時から神経学的な異常がみられる子の場合、半数強(55%)が熱性けいれんからてんかんへと移行します。
はじめて熱性けいれんを起こしたとき、発熱からけいれんが始まるまでの時間が短かった子も、熱性けいれんからてんかんへ移行しやすいといわれています。これは、熱性けいれん再発と重なる要因ですが、やはり、てんかん発作の起こりやすさがてんかん発症と関連しているとみることができます。
この4つの要因がひとつもない子では、てんかんの発症率が1%ぐらいと言われています。つまり、熱性けいれんのない子とほとんど同じです。
この1から4の要因をもっていて、てんかんになる危険性が高いのならば、何とかてんかんになるのを阻止できないかと考えてしまいます。たとえば、てんかん発作を抑える薬を飲みつづけることで、てんかんの発症を抑えられないか、ということです。しかし、これは、得策とはいえません。たしかに、抗てんかん薬を飲み続けることによって熱性けいれんの再発を抑えることはできます。しかし、その後のてんかん発症を阻止できるという保証はありません。また、発症したてんかんの難治化を阻止できるという証拠もありません。抗てんかん薬の副作用を考えると、必ず起きると限ったわけでもないてんかん発症を恐れ、抗てんかん薬をお子さんに飲ませるのは、お勧めできません。てんかんが発症した時点で、きちんと抗てんかん薬で治療を開始しても遅くはありません。その時点で治療を始めても,てんかんの予後の面からも知的な面からも、けっして手遅れではないのです。
熱性けいれんがてんかんの原因になるのではないかという疑問は、保護者の方だけのものではありません。じつは、専門家の間でもずっと議論され続けてきました。前に、熱性けいれんが「悪化」しててんかんになるわけではないと申しあげました。このことは、熱性けいれんのほとんどのお子さんに当てはまりますし、間違いではありません。しかし、きわめてまれに、そうともいえない病態が2つ、熱性けいれんに関連して生ずることが知られています。ひとつが、片側けいれん-片側麻痺-てんかん症候群 (Hemiconvulsion-Hemiplegia-Epilepsy 症候群、略して、HHE症候群)、もう一つが、内側側頭葉硬化てんかんです。いずれも、熱性けいれんが重積状態になることによって生ずる病態です。
片側けいれん-片麻痺-てんかん症候群(HHE症候群)
HHE症候群は、4歳未満の乳幼児にみられる病態です。初発症状は、右半身または左半身がピクピク、ガクガクしていつまでも止まらない発作、遷延性片側間代けいれんです。とめどもなく涎が口から溢れでたり、呼吸が不安定になるといった自律神経の不調を疑わせる症状が発作に付随してみられることもあります。何時間にもわたって発作は続き、へたをすると、24時間を超えてしまうこともあります。しかも、この遷延する発作をなんとか止めることができても、その後に麻痺が残ります。けいれんしていた側の手足がダランとして、力が抜けた状態になるのです。発作後のこのような麻痺をTodの麻痺と呼ぶということは、以前、お話しました。けいれんをもたらす異常電流のために脳の神経細胞がエネルギーを使い果たし、一休みするために起きる、一過性の機能性麻痺です。ところが、HHE症候群では、この発作後の麻痺がいつまでもつづき、最終的に半身不随になってしまいます。Todの麻痺のような機能性麻痺と異なり、HHE症候群では長いけいれんによって脳の神経細胞が破壊されてしまいます。麻痺はその結果として生じますから、元通りには戻りません。頭部のCTやMRIでみると、発作が起きていた側とは反対側の大脳半球の容積が減少しています(図2)。神経細胞が壊れてしまったためです。神経細胞の破壊は運動を司る皮質にとどまりません。言語や記憶に関連する皮質にまで破壊は及びます。このため、知的な障害も残ります。そして、数ヶ月後、数年後に、神経細胞が破壊されて生じた異常神経細胞網において、異常電流が流れはじめます。てんかん発作が起きるようになるのです。それも、きわめて難治なてんかん発作のことがほとんどです。
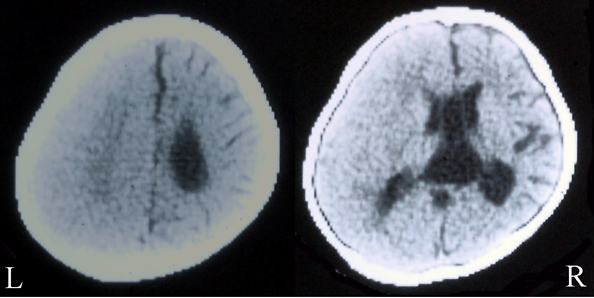
| 図2 3歳半 男児 HHE症候群 3歳半まで発熱に伴う全身けいれんが10回起こっていたが抗てんかん薬の予防投与は行なわれていなかった。38.2度の発熱に伴って全身けいれんがみられ、3時間続いたのち、ジアゼパムの静注で発作はいったん頓挫した。しかし、5分後、左片側けいれんが始まり、種々の治療に抵抗、フェニトインの静脈注射によって3時間後にようやく発作は消失した。しかし、CT上、右半球が委縮し、左半身の弛緩性マヒが残存した。2日後フェニトインの徐脈内投与を中止したところ口唇のピクつきに始まり、眼球左方変異から左上下肢の硬直に進展する発作10回認め、フェニトインの内服を開始し、発作は消失した。3年後、口唇のピクつき、眼球の左方偏視、意識消失を伴う発作が日に数回認められるようになって難治に経過した。 |
このように、遷延する片側けいれんの後に、片麻痺となり、最終的にてんかん発作も合併するので、片側けいれん-片麻痺-てんかん症候群( Hemiconvulsion-Hemiplegia-Epilepsy 症候群、略して、HHE症候群)と呼ばれています。
初発時、片側けいれんに伴って、たいてい、発熱がみられます。しかし、細菌性髄膜炎や脳炎といった発熱をきたし、けいれんを長引かせるような原因はみつかりません。中枢神経感染症などの重篤な原因によらない、発熱を伴う片側けいれんが4歳未満の乳幼児にみられるわけですから、定義上、これは、熱性けいれんということになります。たしかに、HHE症候群は、熱性けいれんが「悪化して」てんかんを起こすようになった病態と表面上はみえます。
HHE症候群の原因はわかっていません。
普通の熱性けいれんに比べると、生まれる前後の仮死に伴う脳障害など、熱性けいれん発症前に脳に何らかの異常があったお子さんが多いことが知られていますが、そうした脳障害をもたずに正常に発達していた子でも起きます。脳に異常のない子にまで、なぜ、それほど長く続く発作が起き、ひどい後遺症を残すのか、よくわかっていません。よくわかっていないのは、じつは、このHHE症候群が先進国では激減していて、ほとんどみられなくなってしまっているのも一因です。半世紀も前、フランスのガストーたちが150例について報告しているのが、HHE症候群についてのもっとも有名な論文ですが、このガストー論文以降、HHE症候群についてこれほど膨大な症例を報告した論文はあらわれていません。少なくなってしまった原因も、病気が事実上消えてしまった今となっては、よくわかりません。しかし、可能性として一番に考えられるのが、遷延する発作、けいれん重積の治療の進歩です。ちょうど、ガストーたちの論文が出てしばらくしたあたりから、けいれん重積を確実に止める治療法が先進国の間で普及し始めました。それ以前は、どれほど長いけいれんをしていても、医者も家族の方も、なすすべがありませんでした。けいれん重積で入院して、けいれんするお子さんの手足をご家族がかわるがわる、何日も、押さえつけているしかなかった、という話を患者さんのご家族から聞いたことがあります。その方はひどい後遺症が残っていますが、そのけいれん重積が起きたのは、ガストーの論文が出た5年後のことです。しかし、論文が発表されてしばらくしたのちに、カットダウンといった手法で、子どもであっても静脈に針を差し込むことができるようになり、ジアゼパムを静脈注射してけいれんを押さえ込む治療が定着し始めました。
けいれん発作が一時間以上続くと、過剰興奮によって神経細胞の細胞膜が変調をきたし、水分が細胞内になだれ込んできて細胞体がふくれあがります。そして、けいれんが長引くと、神経細胞がはじけ、脳組織の一部が壊死に陥ります。残念ながら、さきほどの患者さんにはそうしたことが起こってしまったのだと想像されます。しかし、けいれん重積の適切な治療によって、今では、そのようなことは、まず、起こらなくなってきています。
HHE症候群が消えてしまったのには、もう一つ、理由が考えられます。 HHE症候群の原因はわからないと申しましたが、HHE症候群と診断されていたお子さんには、脳炎・脳症や脳静脈血栓症が隠れていたかもしれないのです。
今ですと、何時間も続くけいれんがあれば、MRIの検査をします。すると、さまざまな異常が見つかり、脳炎、脳症、脳静脈血栓症などの診断が下されます。しかし、MRIがない時代、たとえ疑うことはあっても、病理解剖でもなされない限り、そうした疾患を確定診断することはできませんでした。HHE症候群は髄膜炎、脳炎、脳症などの器質性疾患を除外して診断されていたことは事実ですが、今から考えると、除外しきれていなかった疾患が存在していた可能性を否定できません。しかし、今ですと、そうした症例は、HHE症候群とは診断されません。このことも、HHE症候群が激減した一因をなしているかもしれません。
HHE症候群が激減したというのは、私自身のささやかな経験からの実感でもあります。この症候群を最初に診たのは、30年前、小児科医になりたての頃です。熱性けいれんの既往がある3歳半の男の子が、片方の手足がピクピクする3時間以上続くけいれんで、当時、私が勤務していた病院にやってみえました。ジアゼパムの静注で、一旦、けいれんは止まりました。しかし、しばらくして、再発してしまい、さまざまな薬を使ってもとまらず、結局、思い切ってフェニトインを静脈注射することによってようやく完全にけいれんを止めることができました。しかし、その頃には、すでに、病院にみえてから3時間以上たっていました。けいれんが止まってからも、意識のない状態が半日以上続き、けいれんした方の手足はいつまでもダランとしたままです。上司の先生が「こういう子はね、麻痺が残るんだよね」とおっしゃいました。そして、残念ながら、そのとおりになってしまいました(図2)。「毎年来るんだよ、こういう子が」とその先生は険しい顔をして呟かれました。そういうものなんだ、とその時は思いましたが、ありがたいことに、その後、同じようなお子さんを私は診ていません。その頃、同じHHE症候群の後遺症による難治性てんかんの思春期の女の子の治療もしましたが、HHE症候群の後遺症のある子を診たのも、その女の子をのぞいて、あと、先程述べた方だけです。私の限られた経験だけからいっても、たしかに、HHE症候群は、事実上、姿を消しています。 このような事情ですから、日本も含め、医療レベルがある程度以上に達している国においては、HHE症候群によって、熱性けいれんからてんかんを生ずる恐れはほとんどないといっていいと思います。すぐにけいれん重積の治療を開始すればHHE症候群は起こりえないからです。あるいは、HHE症候群ではなく、脳の炎症あるいは血管障害として診断され、遷延した熱性けいれんとはみなされないのかもしれません。
未解決の問題――熱性けいれん重積発作と内側側頭葉硬化てんかん
このように、けいれん重積の治療がきちんとなされている国では、HHE症候群は、事実上、消失しています。 しかし、もう一つ、「熱性けいれんが悪化して」てんかんになるのではないかと疑われている疾患があります。
遷延する熱性けいれんがみられたあと、ある程度期間をおいて発症してくる内側側頭葉硬化てんかんです。
ただし、HHE症候群と異なり、内側側頭葉硬化てんかんの患者さんは、けいれん後、半身麻痺が残るわけではありません。長いけいれんはあったものの、一見、うまい具合になんの問題も残さずにけいれんは終わってしまったようにみえます。しかし、遷延する熱性けいれんを起こしてからかなり年月がたってから、難治てんかんとなってしまうのです。そして、よくよく調べてみると、何も傷跡を残さず治ったはずなのに、側頭葉の内側が硬く小さく縮こまっていることに気づかれます。
ここで、また、すこし、話が横道にそれることを、お許し下さい。
医者になりたての頃、静岡のてんかんセンターで2週間ほど研修したことがあります。初代センター長の和田豊治先生がまだお元気な頃のことです。当時のてんかんセンターの研修医の仕事は、毎朝、初診の患者さんの病歴をとることからはじまりました。そして、脳波,血液検査などの検査がでそろった昼近く、和田先生がその患者さんを診察されるのです。研修医は和田先生に問診と検査の結果を報告し、和田先生の診察を見学、診察が終わり、患者さんとご家族が出て行かれたあとで、先生のお話をうかがうというのが日課でした。
ある時、診察後のお話しのなかで和田先生は「小児科医がきちんとしていないから、てんかんがひどくなる!」と真っ白なあごひげを怒りに震わせられながら、断言されました。当時、私は小児科医になろうと思っていましたから、先生のこの言葉にひるみました。しかし、ありがたいことに、その後、和田先生の弾劾の矛先は精神科医、内科医へと向かい、ほっと、一息つきました(ちなみに、和田先生は精神科医で、てんかんセンターにみえる前には、東北大学精神科の教授をされていました)。どういう文脈のなかで、和田先生のお話が小児科医断罪論に至ったのか、よく覚えていません。ただ、先生が小児科医に不信感をもっておられた原因については、ひとつ、思い当たることがあります。 それは、熱性けいれんと内側側頭葉硬化てんかんとの関係です。
| 内側側頭葉硬化症群 (17例) | 非内側側頭葉硬化症群 (17例) | 統計的有意差 | |
| 男/女 | 9/8 | 8/9 | なし |
| てんかん発症年齢 | 3~14 (平均、12) | 0~12 (平均、4) | あり |
| 熱性けいれん既往歴 | 13(76%) | 4(24%) | あり |
| 遷延性熱性けいれん既往歴 | 12(71%) | 0(0%) | あり |
| 表1 小児期発症側頭葉てんかん34例において、内側側頭葉硬化が原因の17例と内側側頭葉硬化以外の疾患が原因の17例を比較検討。内側側頭葉硬化群はてんかん発症年齢が高く、熱性けいれん、とくに、けいれん重積をきたす熱性けいれん(遷延性熱性けいれん)の既往が圧倒的に多い。 | |||
内側側頭葉硬化てんかんによる患者さんの中には、昔、熱性けいれんを起こしている方が少なくありません。それも、たいていは、20分以上遷延する熱性けいれんです(表1)。しかも、熱性けいれんの時、右半身または左半身優位の間代性けいれんのことが多いのです。その一連の経過から考えると、遷延する熱性けいれんの「後遺症」として、内側側頭葉硬化てんかんが生じてしまったようにみえます。小児科医が「きちんと」熱性けいれんを治療していれば、こんなことにはならなかったはずだ――今から考えると、どうやら、これが、和田先生のお怒りの原因だったようです。
内側側頭葉硬化てんかんについては他でも触れていますが、熱性けいれんを語るうえで重要なことですので、もう一度、説明しておきます。
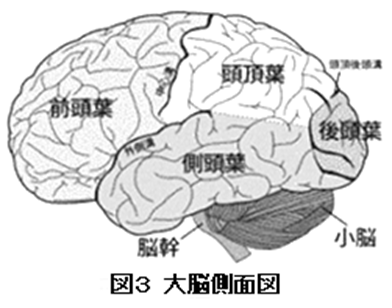
大脳半球は大きな脳溝を境として前頭葉、頭頂葉、側頭葉、後頭葉の4つに区分されています。側頭葉は頭頂葉の下方に前頭葉と後頭葉に挟まれるようにして側頭骨に包まれています(図3)。ただし、それは側頭葉の外側部だけの話です。側頭葉は脳の内側へも入り込んでおり(図6)、この部分も側頭葉に含まれます。側頭骨に接し、外側に位置する側頭葉を外側側頭葉、内側に入り込んだ側頭葉を内側側頭葉と呼んでいます。内側側頭葉は系統発生上古い皮質(旧皮質)で、神経細胞による組織構成も系統発生上新しい(新皮質)外側側頭葉と異なります。
外側側頭葉は他の脳葉同様、数え切れないほどたくさんの機能にかかわっています。しかし、なかでも重要なのが、外界刺激を認識してその情報を処理統合し、過去の記憶と照らし合わせてその意味を判別することです。一方、内側側頭葉にある海馬(図4、6)、扁桃核といった神経細胞集団は視床下部、乳頭体など側頭葉以外の神経細胞群と連帯して記憶に関与しています。また、種の保存に必要な情動や自律神経機能を統合する役割も果たしています。海馬、扁桃核、視床下部、乳頭体は相互に密接に結合しており、記憶形成にも関与しており、辺縁系と呼ばれています。
側頭葉てんかんは、側頭葉に発作焦点があり、側頭葉起源のてんかん発作が繰り返し起きる病態のことをいいます。同様に、発作焦点の部位によって、前頭葉てんかん、頭頂葉てんかん、後頭葉てんかんが区別されます。
内側側頭葉にある海馬、扁桃体といった辺縁系組織は痙攣閾値が低く、てんかん発作焦点を形成しやすい神経集団です。さらに、外側側頭葉に始まったてんかん発射は急速に内側側頭葉に伝播、内側側頭葉で異常電流が励起され、発作が遷延し、他の脳葉に異常放電が拡大していくこともあります。このため、内側側頭葉、とくに辺縁系組織は「てんかん発作のペースメーカー」と呼ばれていたこともあります。
大脳半球の4つの脳葉のうちもっとも大きいのは前頭葉で、脳表の約3分の1を占めます。もし、てんかん焦点になる可能性がどの脳葉でも同一であれば、面積比からいって、当然、前頭葉てんかんの患者さんの数がもっとも多くなるはずです。事実、小児の部分てんかん(症候性もしくは潜因性部分てんかん)では、前頭葉てんかんがもっとも多いといわれています。ところが、成人に達すると、側頭葉てんかんが前頭葉てんかんを抜いて部分てんかん、とくに、難治性部分てんかんのトップに躍り出ます。おそらく、それは、辺縁系内側側頭葉のてんかん発作への閾値が低いことが原因だと思われます(図5)。発作が起こりやすいために、側頭葉てんかんは治りにくく、成人になっても薬で抑えることのできない発作を繰り返すのだと推定できます。このため、成人では、部分てんかん、とくに、難治性部分てんかんといえば側頭葉てんかんというイメージができあがっています。
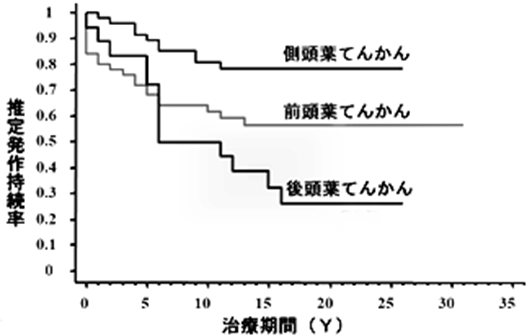
| 図5 小児症候性局在関連てんかんの発作消失率のてんかん類型別経時的変化側頭葉てんかんは前頭葉てんかん後頭葉てんかんに比べ発作消失率が低い。側頭葉てんかんが難治てんかんの主体をなしているのはこのためと考えられる。 |
側頭葉てんかんの病因としては腫瘍、先天性形成異常、瘢痕組織などさまざまなものがあります。しかし、なかでも頻度が高いのが内側側頭葉硬化病変です。
内側側頭葉硬化病変というのは側頭葉内側にある海馬が縮こまって堅くなったものをいいます。手足にひどい傷をすると、傷あとが縮んで堅くなることがありますが、それと似たような感じです。MRIなどの画像では、海馬病変は正常の海馬に比べ縮んでみえます(図6)。組織学的には,海馬の神経細胞が抜け落ちていて,その抜け落ちたあとをグリア細胞という間質神経細胞が埋めています。神経細胞が少ないために、ブドウ糖の消費量が少なく、海馬病変ではブドウ糖のとりこみも低下しています(図6)。
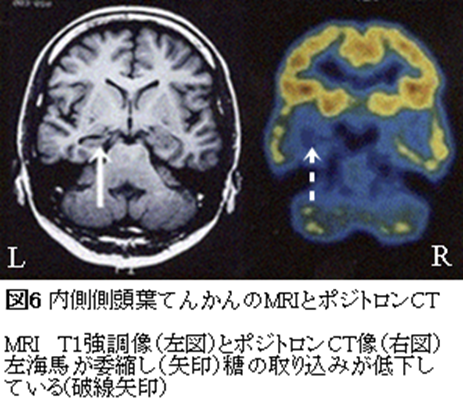
海馬というのは、トビウオの仲間、タツノオトシゴのことです。海馬組織だけを切り出してくると形がタツノオトシゴにそっくりなのでそのように名付けられたようです(図5)(ただし、海馬が何を指すのかということに関しては専門分野ごとに見解が異なります。さまざまな歴史的経緯から解剖学者の多くは海馬をタツノオトシゴではなくギリシャ神話の海の神ポセイドン(ローマ神話ではネプチューン)がまたがっている馬とみなしています。一方、神経病理学者は病理解剖の記事に海馬のことをアンモン角という用語で記載することが少なくありません。エジプトのアモン神の角に似ているというのでつけられた名前で、化石のアンモナイトもこのアモン神から名付けられています。しかし、神経生理学の分野ではタツノオトシゴ説が言い伝えられ、臨床てんかん学もそれにならっています)。
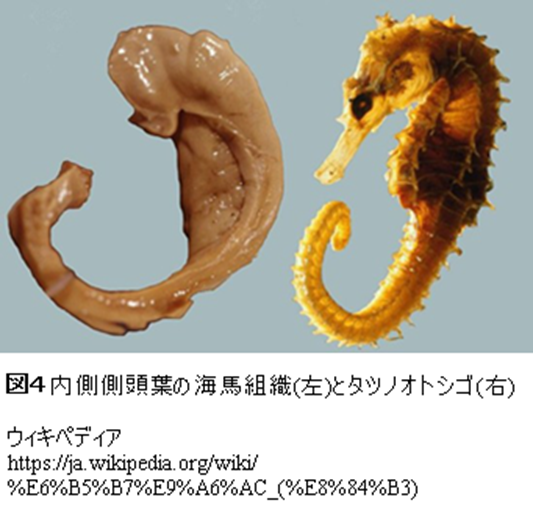
内側側頭葉硬化病変によるてんかん発作の代表的症状は、「胃からこみ上げてくるような」異常感覚です。この前兆の後、意識が飛び、目がうつろとなり、口をもぐもぐさせたり、手に持っているものを弄んだりといった自動症が続きます。この自動症は海馬硬化がある方によくみられる発作症状で、この自動症と同時に、反対側の上肢がゆがんだように硬直することもあります。そして、ときとして、全身痙攣に至ります。こうした発作症状の移り変わりは、内側側頭葉に始まった異常放電が側頭葉全体に広がり、さらには、脳全体に広がっていくさまを映しだしています。 この海馬硬化による側頭葉てんかん,内側側頭葉硬化てんかんは、治療上、重要な特質があります。 表1にお示ししたように、このてんかんは主として幼児期から思春期にかけて発症します。しかし、発症当初は抗てんかん薬の服薬で簡単に発作が止まってしまうことが少なくありません。治療によって、数年、発作がない状態が続き、薬を減量中止できる方もみえます。ところが、その後、しばらくして、発作が再発します。そして、こんどはどんな薬を使っても効きません。前のことがあるので、こんども止まるだろうと患者さんも医者も期待し、いろんな薬を試すのですが、全く効きません。意識が消失する発作が頻回に起き、生活に重大な支障をきたすようになります。
ところが、薬にこれほどの抵抗性であるにもかかわらず、外科治療が驚くべき効果を示します。堅くなった海馬とその周辺のてんかん発作を起こしやすくなった組織を切り取ることによって、80%近くの患者さんで、それまでのことが嘘のように、発作がなくなります。海馬硬化による側頭葉てんかんは、てんかん外科治療によって発作が消失する可能性がもっとも高い疾患の一つで、てんかん外科治療において重要な位置を占めています。
ところで、海馬硬化病変にみられる神経細胞脱落、繊維化ですが、そうした組織変化がどうして生ずるのか、発生機序はまだよくわかっていません。しかし、いずれにしても、前に述べましたように、内側側頭葉硬化てんかんのある患者さんには,熱性けいれん、それも、遷延性熱性けいれんの既往が高率にみられます(表1)。このため、長いけいれんによって海馬硬化が「傷跡」として残ったのではないかという疑惑が生じました。そして、それが、和田先生のお怒りの原因になっていたわけです。「小児科医が熱性けいれんをきちんと治療をしないから、内側側頭葉硬化てんかんのような難治なてんかんになってしまった」というわけです。
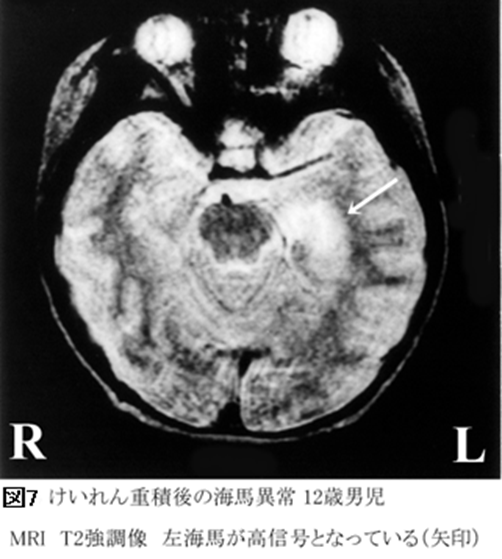
実際、動物実験でも、熱をともなうけいれん重積が海馬の神経網を変化させ、将来、そこがてんかん焦点になりうることが確認されています。さらには、ヒトにおいても、重積けいれんが海馬に異常をもたらす可能性が、MRI検査で確認されています(図7)。
では、長い熱性けいれんは内側側頭葉硬化てんかんの原因といってしまっていいのかというと、それは、ちょっと、早計です。そうともいえない「証拠」があるからです。
NIHなどによる熱性けいれんにかんする前方視的地域研究のデータです。
こうした地域研究では、遷延する熱性けいれんがみられたお子さんのうち,その後、内側側頭葉硬化てんかんになった例がみつかっていないのです。ただし、NIH研究は7歳までのデータしかありません。もっと大きくなったら内側側頭葉硬化てんかんになるこどもがいたかもしれないという反論は、当然、あります。しかし、たとえば、熱性けいれんを起こした子ども329例を平均12年間追跡したのち、MRIを撮像したノルウェイからの報告がありますが、やはり、内側側頭葉硬化てんかんはみつかっていません。しかも、この329例のうち24例は熱に伴って痙攣重積になった例、8例はてんかん発症例です。しかし、いずれの群からも内側側頭葉硬化てんかんはみつかっていないのです。もちろん、12年ではまだ短い、329例では数が少なすぎるという意見もありえます。しかし、少なくとも、熱性けいれんから内側側頭葉硬化てんかんが発症する例は、たとえ痙攣重積になった例に限っても、前方視的地域研究では、まだ、一例も見つかっていないのが現状です。
さらに、内側側頭葉てんかんには皮質形成異常のような脳の先天奇形がときとして合併していることがわかってきました。このことは、熱性けいれん重積状態が内側側頭葉硬化てんかんの原因ではない可能性を暗示しています。つまり内側側頭葉硬化てんかんになる人は、熱性けいれん発症前からなんらかの脳内病変をもっていて、それが原因で乳幼児期に熱をともなうけいれん(それも、遷延性けいれん)を起こし、その後、内側側頭葉硬化てんかんを起こすに至ると考えることもできるのです。しかし、これも推測にすぎません。現在、アメリカでは、多数の熱性けいれん重積例について経時的にMRIを行い、内側側頭葉硬化てんかんが発症しないか確認する研究が行われています。この研究によって、けいれん直後にみられた海馬の腫脹が、一年後には萎縮に転じる例が見つかっています。ただし、そうした例が難治てんかんを発症するかどうかはまだ分かりません。しかし、こうした研究によって、将来、卵(側頭葉硬化てんかん)が先か鶏(熱性けいれん重積)が先かという議論に決着がつく日がくるのかもしれません。
ところが、一方で、最近、内側側頭葉硬化てんかんの手術例が減ってきているのではないという報告もなされています。もしかしたら、1970年代から「きちんとけいれん重積を治療できるようになった」ことが功を奏しているのかもしれません。しかし、これも、きちんとしたデータとして出ているわけではありません。
現時点では、遷延する熱性けいれんによって側頭葉内側硬化てんかんが生ずるかどうかは分からない、と言っておいたほうがよさそうです。
熱性けいれんの生命予後、知能予後
熱でけいれんする我が子の姿を見て、このまま死んでしまうのではないか、死にはしないまでも、脳にひどいダメージを受けるのではないか、と心配される親御さんは少なくありません。しかし、いずれも、杞憂にすぎません。熱性けいれんによる合併症、死亡はきわめてまれです。ほとんどゼロと考えていただいて結構だと思います。膨大な数の熱性けいれん患者を対象とした研究がいくつも行われていますが、熱性けいれんに関連する死亡例は報告されていません。熱性けいれんを起こした子が、その後、知能障害を起こしたり、行動障害をきたしたりすることも、ほとんど、ありません。HHE症候群では知能障害が起こりえますが、きちんとけいれん重積の治療ができる環境にあれば、この症候群が起こらないことは前に述べたとおりです。
数十年前までは、熱性けいれんのある子は知能の遅れや異常行動をきたしやすいと主張する研究者がいました。しかし、これは、熱性けいれん発症前から遅れのあった子、細菌性髄膜炎や脳炎などの重篤な中枢神経感染症でけいれんをきたし、後遺症の残った子、そしてHHE症候群の子を含め、まぜこぜにして考えていたせいです。そうした子を除けば、熱性けいれんのあった子に運動障害が残ったり、知的能力(知能指数、学業成績)の低下を認めたりすることはありません。
兄弟姉妹の間で熱性けいれんがあった子となかった子の知能指数を比較した研究がありますが、熱性けいれん群と非熱性けいれん群の間で差を認めていないのです。熱性けいれんでも複雑型熱性けいれん、あるいは、遷延性熱性けいれん(熱性けいれん重積)を起こした子は、さすがにちょっと劣っているのではないかという気がしますが、そうしたひどい熱性けいれんがみられた子でも、他の兄弟姉妹と比べて知能に差はありません。
熱性けいれんがあった子となかった子の10歳になったときの学業成績、知能指数、行動評価といったさまざまな指標を多数例で比較した研究も行われています。しかし、どの項目においても熱性けいれんがあった子となかった子にく差はありませんでした。さらに、6歳時の比較ですが、熱性けいれんが一回でもあった子は熱性けいれんが全くなかった子と比べて注意力、記憶力の点で差がなかったという報告もなされています。この報告では、ものごとの遂行能力が熱性けいれんの既往がない子に比べすぐれていた、という結論さえでています。
しかし、それでも、2回も3回も繰り返せば、問題が出てくるのではと心配される方もいらっしゃるかもしれません。しかし、少なくとも単純型熱性けいれんでは発作を何度繰り返そうが知的能力に差はでてこないことが確かめられています。
熱性けいれんのお子さんがみえたとき、状態によっては、さまざまな検査を行います。血液検査、微生物の迅速診断検査、MRIやCTといった画像検査、それに、髄液検査です。多くは、発熱やけいれんの原因を調べ、身体の炎症の程度を見積もるためのものです。 そして、このうち、もっとも問題となるのが、髄液検査です。
髄液検査:細菌性髄膜炎を除外するために
発熱をともなうけいれんを起こしたお子さんがみえたとき、なんとしても除外しなくてはならない病気がひとつあります。
細菌性髄膜炎です。
細菌性髄膜炎はまれな疾患ですが、発熱とけいれんをともなうことがあって、表面上、熱性けいれんの病像を示します。その上、熱性けいれんと違い、何もしないと、重大な後遺症を残します。ところが、抗生物質や抗炎症薬によって早く治療を開始すれば無傷ですむ可能性があります。半日、一日の診断、治療の遅れが重大な結果をもたらします。ですから、熱性けいれんの患者さんがみえたときは、真っ先に細菌性髄膜炎の存在を否定する必要があります。ところが、熱性けいれんを起こす乳幼児では、特有の症状が出にくいため。細菌性髄膜炎が見逃されやすいとされてきました。
脳と脊髄を覆う薄い膜を髄膜といいます。細菌性髄膜炎は、この髄膜とその周辺にある髄液、血管などに細菌がとりついて起きる病気です。 消化管や呼吸器などと異なり、脳や脊髄は外界から遮断され、無菌状態に保たれています。この無菌状態の髄膜周囲に細菌が感染すると(細菌は、多くの場合、血液にまぎれ込んで(菌血症、敗血症)、髄膜とその周囲にとりつきます)、髄膜は必死になって脳や脊髄を護ろうとします。強力な炎症反応によって細菌を追い出しにかかるのです。しかし、そううまくはいきません。元々、細菌がいないはずの場所ですから、備えが不十分です。どんどん細菌が増えていきます。そのうえ、自分を護るべき炎症反応が逆に問題をおこすことがあります。細菌が髄膜に忍び込んでくると生体はインターロイキンなどのサイトカインを放出して細菌を撃滅しようとします。ところが、やりすぎてしまうのです。激しい炎症反応によって、逆に、血管が、そして、神経細胞が痛めつけられます。さらに、防御反応によって死滅した細菌の分解物も脳に悪影響を及ぼします。こうしたことから、適切な抗生物質で細菌を殺す手助けをするだけではなく、炎症を抑える薬で炎症反応をコントロールしないと、脳が破壊され、最悪の場合、死に至ります(抗生物質出現以前、細菌性髄膜炎(脳膜炎)は「死の病」でした)。命が助かっても、重篤な運動障害,知能障害、聴覚障害が残ります。 当然、早期診断、早期治療が大切です。時間単位の対応が求められます。
ところが、熱性けいれんを起こす乳幼児のお子さんでは、早め早めの対応が難しいのです。
髄膜に炎症が起きると、高熱、けいれんに加え、髄膜の炎症に特徴的な症状があらわれます。強烈な頭痛、吐き気、嘔吐,異常な目つきなどです。髄膜に細菌がとりつくと、炎症が起こり、その結果、髄膜と脳脊髄の間を流れる髄液の流れが滞ります。脳は頭蓋という骨の閉鎖空間に閉じ込められていますから、行き場を失った髄液は頭蓋内の圧力をどんどん押し上げます。その結果、頭痛、吐き気、嘔吐、眼球運動異常などの頭蓋内圧亢進による症状、徴候がもたらされます。さらに、炎症によって放出されたセロトニンなどの物質によって、髄膜は痛みに鋭敏になります。このため、炎症をおこした髄膜が何らかの形で引っ張られると、異様な痛みを感じ、患者さんの体は防御的に引っ張られまいとします。たとえば、首を屈曲させると、背中側の髄膜が引っ張られますから、首の後側の筋肉に力が入って硬直し、頭を前屈させまいとします。項部硬直と呼ばれる現象です。それでも、無理に首を曲げようとすると、少しでも背部の髄膜の伸展を和らげようとして股関節、膝関節が曲がります。膝がお腹に引き寄せられてくるのです。Brudzinski徴候と呼ばれている現象です。この折れ曲がった膝を無理に伸ばそうとすると、患者さんは首に激痛を感じるため、結局、膝を伸ばすことはできません。これはKernig徴候と名づけられています。これらの症状はいずれも髄膜炎を疑わせる重要な症状や徴候です。中でも、発熱、項部硬直、意識障害は、髄膜炎の三徴と呼ばれています。成人の細菌性髄膜炎であれば、95%の人にこの3徴のうち少なくとも2つがみられます。
熱をともなうけいれんが起きたお子さんでも、こうした髄膜刺激徴候がみられたら、なによりも、まず、髄膜炎を疑う必要があります。そして、背骨の腰の部分、腰椎という椎骨の連なりのすき間に針を刺し入れ、髄液を採取します。髄液に炎症所見がないかどうか、髄液に細菌が紛れ込んでいないかどうか調べるのです。腰椎穿刺と呼ばれる検査です。髄膜炎では、炎症のために髄液の白血球が増え、炎症性タンパク物質が増加し、細菌に消費されて糖分が下がります。髄液にそうした所見がみられ、さらに、細菌がみつかれば、確実に細菌性髄膜炎であると診断できます。診断がついたら、すぐさま、抗生物質とステロイド剤による治療を開始します。
ところが、小児、とくに、乳幼児では、髄膜炎に罹患していても髄膜炎を疑わせる症状、徴候がみられないことがあるとされてきました。年齢が小さいほど症状がはっきりせず、典型的な症状、徴候が出にくいと考えられてきたのです。髄膜炎の三徴がきちんと揃うことなど、乳幼児では、まず、ないと考えられた時代すらありました。
ところが、熱性けいれんにこの細菌性髄膜炎が紛れ込んでいることがあります。熱にともなうけいれんがみられたお子さんの2-5%に髄膜炎が潜んでいる、とかつてはいわれていました。一方、髄膜炎を起こした子どもの13-16%の初発症状がけいれんだという報告がなされています。そのうえ、乳幼児、とくに1歳半未満の乳幼児の髄膜炎では、30-35%で上に述べた髄膜炎に特異的な症状がみられないといわれてきたのです。ですから欧米などでは熱性けいれんがみられた子で、すこしでも髄膜炎が疑われたら、侵襲性の高い検査ではありますが、躊躇なく,腰椎穿刺を行うことが推奨されていました。
たとえば、英国小児科学会は、1991年の熱性けいれんガイドラインで、熱性けいれんを起こした月齢18か月未満の乳幼児、とりわけ、12か月未満の乳児では、腰椎穿刺を行うことを推奨しています。必ずしも、全員に行う必要はないし、経験豊富な医師が臨床所見から腰椎穿刺をやらなくてもいいと判断するならやらないという選択枝があってもいいかもしれないが、しかし、基本的には、少しでも疑いがあるのであれば、やるべきだ、というのです。その後、米国小児科学会も、1996年に、熱性けいれんガイドラインで月齢12か月未満の乳児が熱性けいれんを起こした場合、腰椎穿刺を行うことを強く推奨しています。この月齢では髄膜炎の症状、徴候が全くみられないか、あっても、ほんのわずかだから、というのがその理由です。さらに、月齢12か月から18か月の幼児でも腰椎穿刺を考慮すべきとされています。つまり、1990年代の英米いずれのガイドラインも1歳未満の乳児が熱性けいれんを起こしたら全員腰椎穿刺し、1歳半までの幼児の熱性けいれんでも、腰椎穿刺施行を前提に診療すべきだと勧告していたのです(ちなみに、日本では1996年に熱性けいれんの初のガイドラインがでています。腰椎穿刺について英米のような明確な指示はなされていませんが、やはり、髄膜炎の症状の有無に留意し、「疑いがあれば腰椎穿刺を積極的に施行する」となっていました)。
しかし、では、英米両国においてこの指針がきちんと守られてきたかというと、必ずしも、そうではなかったようです。
たとえば、英国です。
たしかに1970年代には初回熱性けいれんの子どものほとんど(96%)が腰椎穿刺を受けていました。しかし、1980年代に入ると、これが約3分の2(67%)に減少、1990年代には16%にまで激減しています。そして、同じことが、アメリカでも起きています。
施行率が激減した原因のひとつは、腰痛穿刺がかなりの苦痛と恐怖を伴う検査であるためです。しかも、腰椎穿刺は完全に安全であるとは言い切れない検査です。
腰椎穿刺において背中に針を刺す際、お子さんが動くと、針先を狭い髄液腔にきちんと差し込むことができません。このため、お子さんをベッドに横にして寝かせつけ、介助者が両手両足を使ってお子さん押さえ込みます。両足でお子さんの足を挟み込んで動けないようにし、片手で頭を押さえ込み、もう一方の前腕でお腹を押し、腰が突き出るようにします。そうすると、腰椎の骨と骨の間の隙間が空いて、針を差し込みやすくなります。しかし、無理矢理寝かされ、押さえ込まれ、腰にかなり太い針を突き刺されるのですから、幼い子にとってその恐怖、苦痛は並大抵のものではありません。しかも、髄液腔にうまい具合に針先が止まってくれないと、髄液腔壁の血管を傷つけ、血液混じりの髄液を採取することになってしまいます。これでは、髄液をきちんと評価できません。
そのうえ、腰椎穿刺は、全く安全な検査とはいえません。
髄膜炎によって頭蓋内の圧力が高まっているときに腰椎穿刺をおこなうと、きわめてまれですが、死に直結することがあります。腰椎穿刺によって髄液が体外に流れ出て腰の方の髄腔圧が低下し、脳脊髄全体に下向き(尾側向き)の圧力がかかります。このために、脳の中心にある脳幹が頭蓋骨の出口部分で押しつぶされます。脳幹には呼吸や心臓を司る神経集団がありますから、ここが圧迫されると、下手をすると、呼吸運動や心臓の動きが止まってしまう危険性があります(脳ヘルニアといわれる現象です)。ですから、髄液検査は血液検査のように手軽にできる検査ではありません(ただし、細菌性髄膜炎における腰椎穿刺で本当に脳ヘルニアが起こるかどうかについては議論があります。脳ヘルニアを恐れて、必要な腰椎穿刺さえ行われていないことに批判もでています。腰椎穿刺をやってはいけない禁忌事項はわかっているので、それを遵守すれば問題は起きないとされています)。
こうした事情に加え、どうやら、小さいお子さんであっても、細菌性髄膜炎を見逃す可能性が低いことが、わかってきました。これが、腰椎穿刺の施行率を下げているもう一つの大きな要因です。
最初に、熱にともなうけいれんがみられたお子さんでは2-5%に細菌性髄膜炎が隠れている可能性があると書きました。ところが、最近は多く見積もってもせいぜい0.4%、実際にはもっと少ないと推定されています。昔に比べ10分の1以下に頻度が下がっているのです。
原因は予防接種です。
熱性けいれんを起こす乳幼児にみられる細菌性髄膜炎の原因菌の大半は肺炎球菌とインフルエンザ桿菌です(生後4か月から5歳の細菌性髄膜炎を引き起こす細菌は70~72%がインフルエンザ桿菌、20~25%が肺炎球菌でした(日本神経感染症学会作成の細菌性髄膜炎診療ガイドライン)。ですから、この2つの細菌に対する乳幼児の免疫力を高めることができれば、悲惨な結果を招く細菌性髄膜炎の頻度をかなり下げることができるはずです。こうして、欧米を中心として多くの国でこの2つの細菌に対するワクチン(インフルエンザ桿菌b型(Hemophilus influenzae Type b)に対するHibワクチンと肺炎球菌に対するワクチンが開発され、接種されるようになりました。遅ればせながら日本でも、生後6か月までに(できれば2~4か月に)この2つの細菌に対するワクチンを3回済ませる定期接種(4回目の追加ワクチンは1歳を過ぎてから)が行われるようになっています。この結果、乳幼児の細菌性髄膜炎の頻度は劇的に下がりました(数十年前、急性期病院で小児科診療に従事していた頃は、年に1-2回は細菌性髄膜炎の患者さんに遭遇したものです。ところが、最近では、4-5年一般病院小児科に勤務しているのに一度も髄膜炎をみたことがないという小児科医が結構います)。
米国 CDC によれば、Hib ワクチンの定期接種により、5 歳未満のお子さんの Hib 感染症の数は 99%減少したとのことで、発生率は10 万人に 1 人以下になったようです。当然、熱性けいれんに細菌性髄膜炎が隠れている可能性も激減しています。最近の調査では、少なくとも単純型熱性けいれんでは、熱性けいれんに細菌性髄膜炎が隠れている可能性は限りなくゼロに近いということがわかっています。数百例の単純熱性けいれんにおける細菌性髄膜炎発生にかんする検討が欧米のいろいろな施設でなされていますが、どの報告でも細菌性髄膜炎は1例もみつかっていません。おそらく、1000人に1人もいないのではないかと推定されています。 複雑型熱性けいれんでは、さすがに、もう少し、細菌性髄膜炎の頻度が高いようです。526例中3例(0.9%)にみられたという報告もなされています。100人に1人はいると考えておいた方が良さそうです。しかし、そうした場合でも、じつは、熱性けいれん以外に症状がないということは、まず、ない、ということがわかってきています。繰り返し吐いたり、いつまでも意識が戻らなかったり、呼吸状態がおかしかったり、脈が異常だったり、目つきがおかしかったり(目が寄ったり、目が沈み込んだり(落陽現象))、頭の骨の隙間(大泉門)が盛り上がっていたりといった細菌性髄膜炎にともなう頭蓋内圧の上昇を疑わせる症状や徴候が、まず、ほとんどの例でみられることが判明したしてきたのです。
実際、熱性けいれんに細菌性髄膜炎が隠れている場合には、乳幼児であっても、熱とけいれん以外に細菌性髄膜炎を疑わせる症状が付随していることがわかってきています。けいれんに加え、細菌性髄膜炎を強く疑わせる症状がみられるのです。たいていは、いつまでもぐったりとして、反応に乏しく、意識レベルが低下しています。意識レベルが低下していなくても、項部硬直、出血斑など、たんなる熱性けいれんとは思えない症状がみられます。ですから、以前推奨されていたように、1歳以下の初回けいれんであれば軒並み腰椎穿刺をするようなことは必要ないと考えられるようになってきました。それよりも、怪しいと思われるお子さんは入院していただいて、時間をおき、経験のある臨床医が、意識の回復の有無を確認し、髄膜炎を疑わせる症状が出ていないか確認すべきだという考えに傾いてきています。
どうやら、かつての英米のガイドラインは、経験の乏しい研修医であっても細菌性髄膜炎を見逃さない方策として作成されたようです。しかし、結局は、病歴をよく聞き、患者さんの状態をきちんと把握すべき、という本来あるべき臨床診断の姿に戻ってきているわけです。
ただし、アメリカでは、インフルエンザ菌や肺炎球菌のワクチンをうけていない、あるいは、この2つのワクチン歴が不明の6か月から12か月の乳児の熱性けいれんでは腰椎穿刺を選択枝の一つに数えるようにというガイドラインが、米国小児科学会からだされています。さらに、発熱で以前に受診して抗生物質を服用している乳児でも腰椎穿刺を考えるよう呼びかけています。こうした考え方がアメリカに残っているのは、日本と異なり、アメリカでは、保険の関係で、簡単に入院させるわけにいかない、しかし、一方で医療訴訟が多いという事情が隠れているようです。ワクチン未接種、抗生剤の服用が細菌性髄膜炎の発症や見逃しに関係しているという確固たるデータがあるわけではありません。
ということで、日本小児神経学会の熱性けいれん(熱性発作)診療ガイドライン2023では「1.髄液検査をルーチンに行う必要はない、2. 髄液刺激症状、30分以上の意識障害、大泉門膨隆などの細菌性髄膜炎をはじめとする中枢神経感染症を疑う所見を認める例では髄液検査を積極的に行う」ことを推奨しています。日本の場合、ほとんどの医療機関にCT装置があるので、髄液検査施行前、頭部CT撮影で極度の頭蓋内圧亢進をきたす疾患や病態が存在しないことを確認できるだろうという期待も含めた方策なのでしょう。
画像検査
その頭部CT撮影ですが、頭蓋内圧亢進の原因のみならず、痙攣の原因として、脳の異常がないことを確認するのには役立ちます。けいれんの最中に頭を打った可能性がある場合、あるいは、発作後、いつまでたっても目の動きがおかしいといったときには、CT撮影もしくはMRI撮影をやってみる価値があります。しかし、それまで順調に育ってきた子に単純型熱性けいれんがみられ、発作のあとの朦朧とした状態からすぐに回復して平気な顔をしている場合にまでそうした画像検査をするのは、ちょっと、考えものです。異常がみつかる可能性が、まず、ないからです。さらに、CTでは通常のレントゲン検査の数倍の量の放射線を浴びることになります。一方、MRIは時間がかかるために、小さいお子さんですと、睡眠薬で寝てもらわなくてはいけません。しかし、これが、絶対に安全とはいえません。それなのに、異常所見がみつかる可能性がほとんどないのですから、割が合いません。もし行うとしたら、片側けいれんのような明らかな焦点性発作がみられたときや、遷延性発作がみられたときだけでしょう。その場合、CT撮影よりもMRI撮影のほうがおすすめです。放射線を浴びずにすみますし、異常所見の検出率も高いからです。
脳波
熱性けいれんの主症状はてんかん発作ですから、てんかん同様、脳波が重要な検査とお思いかもしれません。
しかし、熱性けいれんにおける脳波の活躍の場は限られます。
もちろん、熱性けいれんを起こしている最中に脳波を記録できたら、相当な価値があります。熱にともなって間違いなくてんかん発作が起きていることが確認できますから。「てんかんと似て非なるもの」のところで述べたように、熱性けいれんは熱性失神などさまざまな発作性疾患との鑑別が必要です。ですから、てんかん発作であると確実に診断ができることは大切です。しかし、前に述べましたように、熱性けいれんにおいて発作中に脳波が記録されることはめったにありません。ほとんどの場合、発作時脳波の助けはえられず、発作を目撃した人の話を詳しく聞いて、熱性けいれんかどうか判断することになります。そして、また、それで十分です。
脳波は、熱性けいれんが長引いているときにも有用です。痙攣が長引いていれば、点滴で血管を確保し、すぐに、抗痙攣剤を血管内に入れて、発作を止めます。しかし、症状から、本当に発作が長引いているのかどうか疑問を感じるようなことが、たまに、あります。そうした場合には、脳波をとる必要があります。
というのは、熱性けいれんを起こすお子さんの中には、けいれんが終わった後もボーっとして、意識がなかなか戻らず、さまざまな「けいれん様」の異常な動きを数十分にわたって示すことがあり、本当に発作が止まったのかどうかわからないことがあるからです。「痙攣性運動を伴う遷延性非てんかん性もうろう状態」と呼ばれる状態です。この「けいれん様」異常運動というのは、強直姿勢、全身の筋緊張亢進、焦点性間代、眼球偏位、自動症様運動で、一見、てんかん発作(複雑部分発作)みたいにみえます。しかし、顔色は悪くありませんし、最初は刺激しても反応にとぼしく、意識が低下しているようにみえますが、そのうち、だんだん反応がみられるようになります。けいれん重積状態のようにみえるのですが、脳波をとってもθ波,δ波といった不規則な遅い波がみられるだけで、てんかん発作時に特徴的な律動波はみられません。代わりに、睡眠から目覚めるとき小さい子によくみられるような不規則徐波がみられるのです。このことは、この痙攣様異常運動が異常覚醒反応状態である可能性を示唆しています。このようなてんかんを疑わせる症状を伴う遷延性非てんかん性もうろう状態は脳波をとれば一目でわかります。
さらに、発作が止まってしまっていても、けいれんのすぐ後であれば、脳波をとる意味が少しあります。発作によって脳が疲れ、遅い波がでていることがあるからです。脳のエネルギーを消耗させるような何かが起きたことを示唆する所見です。その何かは、てんかん発作である可能性が高いと考えられます。こうした「遅い」波は熱性けいれん後1週間近くまでみられます。
また、もし、患者さんの意識がいつまでたっても戻らず、脳波上、きわめて遅い波が続いていたら、これは、大変です。脳炎、または、脳症を発症しているおそれがあります。発熱もけいれんも脳炎、脳症の一症状だったのかもしれません。こうなると、脳波が大活躍します。脳炎、脳症における脳の機能異常の経過を見るためにも、けいれんの再発を発見するためにも、脳波はきわめて大事な検査です。必要に応じて、脳波をしばらく連続して記録することもあります。
しかし、通常の熱性けいれんでは、急性期を過ぎて、一週間後、一ヶ月後になると、脳波の価値はずっと下がってしまいます。
この時期に脳波をとる理由としては2つ考えられます。一つは、熱性けいれんをきたす原因として脳の異常が隠れていないかどうかの確認です。とくに、けいれんが長引いたり、何度も起こったりといった複雑型熱性けいれんのお子さんの場合、気になるところです。しかし、脳の構造異常の確認に、脳波はあまり役に立ちません。それまでの発達歴や神経学的所見の方がよほど脳の構造異常の有無の判定には役に立ちます。そして、もし、それらで何か疑われるのであれば、脳波ではなくMRIなどの画像検査をやるべきです。
もうひとつ、将来、てんかんにならないかどうかを脳波で予測できるのではないかという期待もあるでしょう。ところが、こちらも、予測できたらどうするかということまで考えると、脳波はあまり有用とは言えません。
たしかに、熱性けいれんのない子に比べ、熱性けいれんのある子は脳波異常、とくに、てんかん放電がでやすいのは事実です。しかも、3歳、4歳と年を重ねるごとにてんかん放電がみられる頻度が高まります。そして、熱性けいれんでは脳波異常がみられるとてんかん発症の確率が高まるという報告も結構あります。たとえば、熱性けいれん罹患児179例を追跡したところ、全般性脳波異常がみられた6.7%、焦点性異常のみられた33%にてんかんが発症したという報告がなされています。
しかし、問題はそこからです。
脳波異常がみられるとてんかん発症の可能性が高いのはわかったが、では、それがわかったからといって、何か役に立つでしょうか。
たとえば、てんかん発症率が高い焦点性異常がみられたとして、だから、発症予防のために抗てんかん薬を飲むかどうかです。
これが得策でないことはすぐにお分かりだと思います。てんかん発症率が高いといっても約3分の1のお子さんだけです。後の3分の2のお子さんはてんかんを発症しないのです。
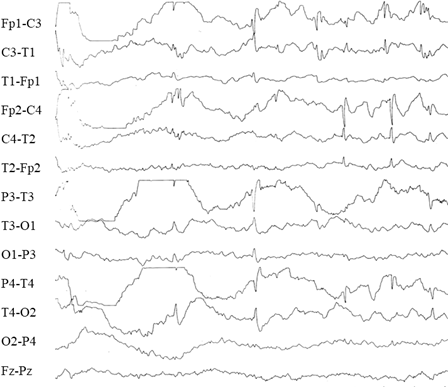
| 図8 ローランド棘波:ローランド溝周囲の中心-中側頭部(C3、C4~T3、T4)に頻回に認める棘波 |
熱性けいれんの子にみられる典型的な焦点性脳波としては、睡眠中、中側頭部に頻繁に現れるローランド棘波があります(図8)。この脳波異常がみられる子は、口がゆがみ、よだれが出るシルビウス発作や全身けいれんを起こすことがあります。しかし、前にも言いましたように、この異常脳波は、ある意味、てんかん性素因を表すものに過ぎず、てんかん発作を起こさない子も半数ぐらいいることがわかっています。これは、熱性けいれんの子でも変わりません。てんかんを発症するとは限らないのです。さらに、てんかん発作を起こしたとしても思春期ごろには発作はみられなくなりますし、それに、発作を起こそうが起こすまいが、知的機能などに影響を及ぼさないことがわかっています。
一方、全般性異常脳波ですが、これで紛らわしいのが、入眠期に出現する小さな棘波を伴った突発的高振幅不規則徐波活動です。欠神発作(Petit mal)の時に脳波でみられる棘徐波に似て非なる脳波パターンということで、昔、Pseudo petit mal variantsとも呼ばれたこともある脳波所見です(図9)。てんかんとの関連が疑われた脳波所見ですが、結局、熱性けいれん児に特有な脳波所見にすぎないことが判明しました。熱性けいれんの既往のある子の4分の1にみられますが、てんかんとの関連は薄いことがわかっています。しかし、脳波所見からてんかんと診断されて抗てんかん薬を服用している子が昔は結構いました(今も、いるかもしれません)。こうなると、脳波をとること自体が害をもたらすことになってしまいます。
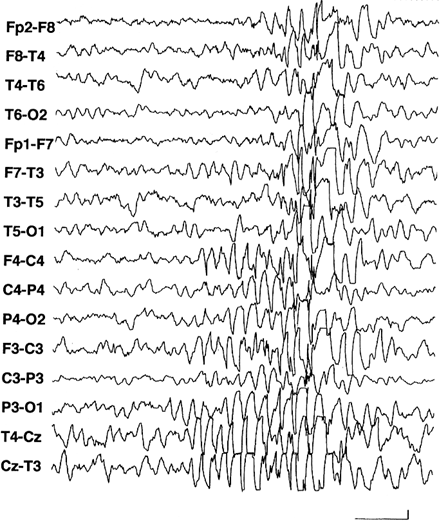
| 図9 Pseudo petit mal discharges:熱性痙攣の子によく認められる低振幅棘波を伴う突発性高振幅不規則徐波活動。Rudimentary spike wave complexとも呼ばれる。 |
一方、熱性けいれんの再発を脳波が予測してくれるかもしれないという考えもあるかもしれません。しかし、これも期待を裏切ります。脳波に異常があった例となかった例で熱性けいれんの再発率に有意な差はなかったという報告がなされています。
というわけで、熱性けいれんの子で脳波をとる必要はあまりないと現在のところ考えられています。それどころか、神経学的異常のない単純型熱性けいれんの子では、脳波をとってはならないという意見さえあります(米国小児科学会)。脳波をとって異常がみられたとしても、それによって何か有効な対策が立てられるわけではなく、保護者の方の心配の種を増やすだけというのがその理由です。下手をすると、それで、無意味な抗てんかん薬の服薬につながるかもしれず、有害無益だというのです。
血液検査
熱性けいれんに対する血液検査としてはナトリウム、カルシウム、リン、マグネシウムといった電解質、あるいは、血糖、白血球数などの測定が考えられます。しかし、必須ではありません。たしかに、脱水、電解質異常、低血糖でけいれんが起きることがあります。しかし、きわめてまれですし、病歴からそうした異常が疑われるときだけ血液検査をすればすむことだ、という意見がとくにアメリカあたりでは主張されています(皆保険ではなく、安易に血液検査ができないというアメリカの医療事情があるせいだと思われますが、しかし、最初から検査ありきではなく、まずは病歴をしっかりとって患者さんをきちんと診るべきだ、という意味では傾聴すべき意見でしょう)。吐いて、ひどい下痢をして、皮膚の張りがなくなっている(ツルゴール(皮膚の弾力)の低下がみられる)、尿が減っている、いつまでも意識障害が回復しないといった症状、徴候をまず拾い集めて考えよう、ということです。特有の症状がみられるという意味では低血糖も同じで、該当症状がみられれば当然血液検査を行いますし、逆に、そうした症状もないのに機械的に検査をやる必要はないということです。
ただし、熱性けいれんの子には血液のナトリウム濃度が低く、そういう子は、同じ発熱時にもう一度けいれんを起こしやすいという報告がなされています。しかし、そんなことはないという結果を報告している論文もあり、今のところはっきりしません。しかし、いずれにしても、ただでさえ低いナトリウム濃度の血液をさらに薄めてしまう恐れがありますから、熱性けいれんの子にやたら水を飲ませてあげるのはやめた方がいいでしょう。どうしても飲ませたいというのであれば、ナトリウムを含むスポーツドリンクかジュースの方がいいでしょう。
ということで、血液検査をやるとしたら、ほとんどが、けいれんの原因ではなく、熱の原因を探るのが目的です。しかし、その場合でも、対象となるのは、たんなる熱性けいれんではないと思われる複雑型熱性けいれんの子がほとんどです。単純型熱性けいれんが起き、病歴や付随症状にとくに何も問題がない子では、やはり、無理やり針を刺して血液を採る必要はないとされています。
高熱(39℃以上)の小さな(3歳未満)子には血液に細菌が入る菌血症が多いことが知られています。熱性けいれんでは高熱のことが多いですし、その上、けいれんまで起こっているので、熱性けいれんの子には菌血症が多いように思われがちです。実際、頻度は多くはありませんが、そうした報告がなされています。しかし、同じような熱の高さであれば、菌血症は熱性けいれんの子にとくに多いわけではありません。けいれんを伴わない高熱のお子さんの菌血症の頻度と変わりません。菌血症の子は白血球数が多い(15,000/mm3以上)ことが知られていますが、熱性けいれんだからといって白血球数を測り、血液の培養をしなくてはならないということではありません。やはり、他の症状も勘案して判断すべきことです。けいれん同様、原因疾患の鑑別も症状、徴候が出発点になります。
熱性けいれんの発熱はさまざまなウイルスや細菌によって引き起こされます。現在、インフルエンザウイルス、ロタウイルス、RSウイルス、アデノウイルス、コロナウイルス、ヒトメタニューモウイルス、溶血性連鎖球菌などさまざまな微生物の感染の有無を鼻やのどの拭い液や、便などを使って素早く調べることができます。数十分程度で測定が完了し結果がでることから、迅速検査と呼ばれています。熱の原因を調べるために、時として、こうした検査が行われることもあります。発熱の原因を調べるのであれば、その地域の感染症の流行状況を勘案してこうした迅速検査をやった方が早道だからです。
熱性けいれんの治療は2つにわけて考えると整理しやすいでしょう。 ひとつは熱性けいれんが起きた直後の急性期治療、もうひとつが、再発防止のための予防的治療です。
最初に申しましたように、熱性けいれんを起こした子のほとんどは救急外来に着いた頃には発作が止まっています。ボーッとしていたり、眠っていたりと発作後の症状はさまざまですが、いずれにしても、発作そのものに対する治療は、とりあえず、必要ありません。
同様のことが、熱の原因についてもいえます。熱性けいれんにおける発熱の原因は突発性発疹症などのウイルス感染症がほとんどです。何もしなくても、自然に熱はおさまりますし、せき、鼻水などの付随症状も消えていきます。それに、細菌感染と違い、ウイルス感染は抗生物質が効きません。インフルエンザウイルス、ヘルペスウイルス、RSウイルス、コロナウイルスなどを除くと、ウイルスの増殖を抑える薬はなく、発熱に対しても、解熱剤で症状の軽減を図るぐらいのことしかできません(ちなみに、解熱剤にはけいれんそのものにたいする再発予防効果はありません。一方、解熱剤で一旦熱が下がったあとに、また、急激に熱が上がると発作を誘発するのではないかと心配になりますが、これも、杞憂にすぎません。ですから、お子さんを楽にして、食欲を回復してあげるために安心して解熱剤を使ってください。もちろん、使いすぎるのも考えもので、次に使うときは、せめて6時間以上はあけましょう)。
ただ、まれに、けいれんがいつまでも止まらず、救急外来におみえになったときも、けいれんが続いていることがあります。もちろん、そんな場合は、一刻も早くけいれんを止める必要があります。静脈内に針を留置して点滴ルートを確保し、ジアゼパム(セルシン注射液、ホリゾン注射液)やミダゾラム(ミダゾラム注射液)といったベンゾジアゼピン系注射液を静脈内に入れてけいれんを止めます。5分程度のけいれんならまだいいですが、何十分、何時間もけいれんが続くと、前に申した片側けいれん-片麻痺-てんかん症候群のように、後遺症を残すおそれがでてきます。
重積状態の熱性けいれんのほとんどは、ジアゼパムやミダゾラムの静注によって抑えることができます。万が一こうしたベンゾジアゼピン薬剤が無効であっても、フォスフェニトイン、レベチラセタム、フェノバルビタールなどの注射液があとに控えています。よほどのことがない限り,遷延する熱性けいれんは止めることができます(止まらなければ、まれですが、脳炎、髄膜炎、脳腫瘍、乳児重症ミオクロニーてんかんなどの重篤な疾患が隠れている恐れがあります)。
しかし、こうした処置は 病院においてしかできません。家で何とかできないのかと思うのは当然ですが、現状では、うまい方法がありません。ジアゼパムの座薬(ダイアップ座剤)がありますが、挿入してから有効な血中濃度に達するまでに最低30分はかかりますし、座薬が便の中に入ってしまった場合、腸からの吸収に時間がかかって、発作はさらに長引く可能性があります。もう一つ、抱水クロラールの座薬(エスクレ座剤、エスクレ注腸用キット)があり、発作を止められる可能性があります。しかし、残念ながら熱性けいれんの重積状態に有効かどうかきちんと検討したデータがなく、あまり使われることはありません。
結局、5分以上発作が続くようなら、迷わず救急車を呼ぶか最寄りの医療機関にかかるのが、現時点ではもっとも賢明な方法といえるかもしれません。しかし、医療機関へのアクセスが全国一律ではないので、一概にそうとも言い切れず、けいれん重積の恐れのあるお子さんについては、上に述べた方策を主治医の先生と相談しておくのがいいでしょう(2020年12月にミダゾラムの口腔内投与薬、ブコラムが市販されました。ミダゾラム口腔内投与はジアゼパム静注と同等の効果があり、手技の簡便さから、ジアゼパム静注より早く効く可能性があるといわれているので、熱性けいれんの対応においても変革をもたらすものと期待されます。しかし、まだ、臨床データが十分には集積しておらず、2023年熱性けいれん診療ガイドラインではこの製剤の活用法は定式化されていません)。
熱性けいれんの3分の2は、再発しません。再発するのは残りの3分の1だけです。この頻度を高いとみるか低いとみるか、発作の激しさにもよりますから、判断が難しいところです。再発の危険因子が色々あることはさきほど述べました。しかし、それらを考慮に入れても、再度発作を起こすかどうかを正確に予測することはできません。そこで、何とか再発を防止する方策が検討されてきました。
わが子のひきつけるさまを二度と見たくない、ということでしたら、抗てんかん薬を連日服用するのが一番確実です。実際、数十年前までは、熱性けいれんに対する治療として抗てんかん薬を連日服用することが結構行われていました。フェノバルビタール(フェノバール,ルミナール)やバルプロ酸(デパケン、ハイセレニン、セレニカR)を毎日服用すると無投薬の場合に比べ再発率が低下することがわかっています。最終発作から1-2年,または,4-6歳までを目安として薬を飲み続ける、というのが標準的服用法です.
しかし、現在では、熱性けいれん予防再発のためのこうした抗てんかん薬の連日服用は、ほとんど、行われていません。抗てんかん薬の副作用や抗てんかん薬を飲み続ける手間を考えると、割にあわないからです。有効といっても、抗てんかん薬の連日服用によって熱性けいれん再発を完全に阻止できるわけではありません。初回熱性けいれんの再発率は30%強ですが、それを10%前後に下げられるにすぎません。それに、飲まなくても3分の2は二度と発作は起きないのです。副作用を考えると(最低でも30%にみられるという報告があります)、少なくとも、一回目の熱性けいれん後に始めるべき治療法とは思えません。しかし、それでも、次の発作をどうしても阻止したいのであれば、次に述べる間欠的投与という方法があります。こうしたことから、現在は、きわめて限られた熱性けいれんの患者さんにしか抗てんかん薬の連日投与はなされていません。たとえば、遷延する熱性けいれんを何度も繰り返していて、次に述べるジアゼパムの間欠投与でも再発を抑えられないような場合です。
なんの前触れもなく発作が起きるてんかんと異なり、熱性けいれんでは発熱という危険信号が点灯します。そこで、危険信号が発せられた時だけ抗てんかん薬を使って発作を予防できないか、という考えが、当然、でてきます。
ところが、これがけっこう難しいのです。
まず、熱に気づいたとき、確実に薬を体の中に入れなくてはなりません。しかし、熱で不機嫌で、食欲もおちている赤ちゃんや幼い子は薬を飲んでくれないかもしれません。飲んでくれなければ、口以外から薬を入れるしかありませんが、その場合、口の反対側、肛門から座薬を入れることになります。しかし、うまくお尻から薬を入れることができても、その薬が直腸粘膜からすばやく吸収され、けいれんを起こさないだけの脳内濃度に到達して抗けいれん作用を発揮してくれなくては困ります。熱性けいれんの2割は発熱してから1時間以内に発作が起きますから、せめて10分か20分で体内に吸収され、十分な脳内濃度に達する薬が望まれます。
このような条件にかなう薬が、ジアゼパムです。日本では、ダイアップ座剤(4mg、6mg、10mgのものがあります)という名前でジアゼパムの座薬製剤が発売されています(抗てんかん薬の座薬としては、もう一つ、ワコビタール座薬がありますが、これは、フェノバルビタールの座薬製剤で、ジアゼパムのように素早く有効濃度に達しませんので、熱性けいれんの予防には使えません)。
熱に気づいて、ダイアップ座剤をすぐにおしりに入れると、熱性けいれんの再発率が3人に1人から10人に1人、1割に低下します。
たしかに、有効なのです。
しかし、現在、この方法も、あまり、推奨されていません。
なぜかといいますと、まず、「熱に気づいたとき」というのが曲者です。口で言うのは簡単ですが、熱に気づいてからダイアップ坐薬を肛門にいつもうまく挿入できるとは限りません。そもそも、熱に気づかない可能性さえあります。けいれんを起こしてはじめて熱に気づかれることが熱性けいれんではめずらしくありません。さらに、熱に気づいても、肝心のダイアップ坐薬が手元にないかもしれません。あっても、処方されてから年数がたっていて、使用期限が切れているかもしれません。
そんなこんなで、熱に気づいても、座薬を入れられないかもしれないのです。じつは、ダイアップで発作再発率が3分の1から10分の1に減ったというのは「きちんとダイアップ座剤を入れられた」例に限ったデータです。「きちんとダイアップ座剤を入れられなかった」例も含めてしまうと、ジアゼパム坐薬を処方された場合の熱性けいれん再発率は、処方されていない場合とたいして変わらないという結果がでています。
さらに、副作用の問題があります。昔、発熱時のダイアップ座剤挿入が熱性けいれんの予防として行われ始めた頃は、発熱に気づかれた時点で一回ダイアップを挿入し、8時間後、まだ、熱があったら、もう一回、挿入するという方法が推奨されていました。そうすれば、ジアゼパムの抗けいれん効果を24時間保つことができ、熱性けいれん再発をかなりの確率で防ぐことができるはず、というもくろみからです。しかし、これをきちんとやろうとすると、大変です。熱があるうえに、ダイアップのせいで眠気がひどく、ふらつき気味、ぐったりして、ご飯も食べられません。逆に、異常に興奮することもあります。こんな副作用が10人のうち4人にみられます。
発作が起こさないようにするために、本当にここまでやらなくてはいけないのか、かなり、疑問です。それに、薬でボーッとしているため、髄膜炎の症状と見間違えるおそれもあります。だいいち、もともと、何もしなくても、3分の2は発熱しても発作は起きないかもしれないのです。とても、きちんとやる気にはなりません。そんなこんなで、現在、単純型熱性けいれんでは再発回数が多い場合を除き、ダイアップ坐薬の間欠投与はほとんど行われていません。
しかし、では、複雑型熱性けいれん、とくに、いつまでもけいれんが止まらないような場合、どうすればいいんだという心配が残ります。てんかん発作が止まらないとき、前に述べたように、病院では、患者さんの静脈内に針もしくはカテラン針を刺し、ダイアップの主成分であるジアゼパムの注射液(セルシン、ホリゾンなど)などを血管に入れて、発作を頓挫させます。しかし、もちろん、家では注射はできません。そこで、速効性を考えるなら、ジアゼパムの注射液を直腸に入れるのが次善の策ということになります。ジアゼパムはすぐに直腸粘膜から吸収されて血液内に入り、脳内に取り込まれます。そして、直接、血管に入れた場合と遜色がないほどの抗けいれん作用を発揮します。今では、これで十分ということになっています。しかし、日本では直腸挿入用のジアゼパム液は市販されていません。代わって、ジアゼパム坐薬(ダイアップ坐薬)を入れるのですが、しかし、ジアゼパム坐薬はジアゼパム液ほど吸収が早くありません。ですから、けいれんが長引いていれば(5分以上であれば長いといえます)、まず、救急車を呼び、そのあと、ジアゼパム坐薬を入れ、最寄りの総合病院に連れて行ってもらうことになります。先ほど述べたミダゾラムの口腔内投与(ブコラム)がこういう時一役買ってくれそうですが、データが蓄積されていないため、実際にどのように使うすべきかの提案がまだなされていません。
ということで、熱性けいれんの予防法は、まだ、きちんと定式化できていません。再発する危険性、再発した場合の影響がひとりひとり異なるためです。たとえば、1歳未満の赤ちゃんであれば、再発する可能性は5歳の幼児に比べ高いでしょう。前回、何十分もの長いけいれんで、救急車で病院を受診、何とかけいれんを止めてもらったのであれば、次回のけいれんはなんとしても止めたいところです。さらに、医療環境にもよります。発作が長引いても救急車ですぐに急性期病院に受診できるのであれば、無理をして予防する必要はないかもしれません。そうした個々の事情を考慮して定式化したガイドラインは、残念ながら、まだ、できていません。
| メモ2 熱性けいれんのジアゼパムによる予防投与適応基準 日本小児神経学会 熱性けいれん(熱性発作)診療ガイドライン2023 1.熱性けいれんの再発予防の有効性は高い。しかし、熱性けいれんの良性疾患という観点と高い有害事象の出現から、ルーティンに使用する必要はない 2)以下の適応基準1)または2)を満たす場合に使用する 適応基準 1)遷延性発作(持続時間15分以上) または 2)次のi~viのうち二つ以上を満たした熱性けいれんが2回以上反復した場合 i. 焦点性発作(部分発作)または24時間以内に反復する発作の存在 ii. 熱性けいれん出現前より存在する神経学的異常、発達遅滞 iii. 熱性けいれんまたはてんかんの家族歴 iv. 初回発作が生後12か月未満発熱後1時間未満での発作の存在 v. 38℃未満の発熱に伴う発作の存在 |
今のところ、どの国のガイドラインでも意見が一致しているのは、単純熱性けいれんが1~2回起きたからといって予防する必要はない、ということぐらいです。
しかし、日本小児神経学会の熱性けいれん診療ガイドライン2023ではメモ2に挙げた条件を満たせばジアゼパム坐薬による予防投与を考慮しても良いのではないかと提言しています。なぜ、この条件なのかは、ここでは詳しく説明しませんが、今まで述べてきた熱性けいれんの危険因子が含まれていることはご了解いただけると思います。たとえば、Shinnarは遷延する熱性けいれん、一回の発熱時に何度もけいれんを起こす熱性けいれん、年齢などの理由から再発の可能性が高い熱性けいれん、離島のように緊急時にすぐには医療機関が受診できないかもしれないお子さんの熱性けいれんに対しては、再発予防のために、あるいは、けいれん発生時にジアゼパムの直腸内投与をしてもいいのではないかと述べています。このような意見がこのガイドラインの適応基準に反映していると思われます。
ちなみに、前にも申しましたが、解熱剤にはけいれんを止めたり、予防したりする力はありません。熱を下げるために体を冷やしても同様です。もちろん、熱が高く、不機嫌だったら熱を下げてあげたくなるのは当然です。しかし、その場合でも、ジアゼパム坐薬を使うのであれば、30分は解熱剤の座薬を入れるのを待って下さい。解熱剤座薬をあまり早く入れるとジアゼパムの吸収が遅れてしまうからです。順番として、ジアゼパム坐薬が先、解熱剤が後です。
表 2 熱性けいれんの再発予防に対して試みられた治療法(Knudsen PU (2002)を改変)
| 投与方法 | 薬剤 | 効果 |
| 持続投与 | フェノバルビタール | 有効 |
| バルプロ酸(デパケン、ハイセレニン、セレニカR) | 有効 | |
| 発熱時 間欠的投与 | ジアゼパムの服用、直腸内投与 (セルシン、ホリゾン、ダイアップ坐薬) | 有効 |
| ジアゼパム以外のベンゾジアゼピン薬剤(ニトラゼパム、クロバザム、ミダゾラム)の服用または直腸内投与 | おそらく有効であろうが、データがほとんどない | |
| 抱水クロラ-ル(エスクレ坐剤) | 有効という報告はあるが,データがほとんどない | |
| 発作開始後 投与 | ジアゼパム注腸(日本にはない) | 対照群を設定しない試みで有効という報告がある |
| ジアゼパム坐薬(ダイアップ坐薬) | 有効だが、効果発現に20-30分かかる | |
| ミダゾラムの頬粘膜、鼻腔内投与 | 有効だが、データが十分ではない |
この薬は避けた方がいい?
解熱剤は発作の再発予防には力を発揮しませんが、逆に、再発を助長するかもしれない薬もあるので紹介しておきます。
抗ヒスタミン剤とキサンチン製剤です。
いずれも、熱性けいれんを悪化させる可能性があると言われています。
抗ヒスタミン剤はアレルギー症状に使われる薬です。ヒスタミンHistamineは肥満細胞、白血球、消化管細胞、神経細胞において炎症反応、胃酸分泌、神経伝達調節などに関与する生理活性物質で、標的細胞の細胞膜にあるH1、H2、H3、H4という4つの受容体を介して効果を発揮します。H1受容体は炎症反応、アレルギー、H2受容体は胃酸分泌、H3受容体は神経伝達、H4受容体は免疫調整に関係しています。このうち、ここで関係が深いのがH1受容体です。ウイルスなどの微生物あるいは花粉などの異物が身体に侵入してくると肥満細胞、白血球などが体を守るためにヒスタミンを吐き出します。そして、このヒスタミンがH1受容体を介して血管などを活性化し、血管拡張(皮膚の発赤)、血液の液体成分の血管外漏出(浮腫)、疼痛を引き起こすのです。その結果として、鼻水、クシャミ、蕁麻疹、皮膚発赤、喘息、発熱などの症状がみられるようなります。こうした症状を和らげるために使われるのがH1ヒスタミン受容体をブロックする抗ヒスタミン剤です。風邪薬や花粉症の薬に含まれていて小児科や耳鼻科などでよく使われている薬です。ところが、脳の神経細胞にはH3受容体があって神経細胞の興奮性を調節しています。その調節が抗ヒスタミン剤によって邪魔されると、抑制機能が阻害され、理論的には、けいれんが誘発されるおそれがあります。とくに、中枢神経を抑制するGABA(γアミノ酪酸)システムの発達が未熟な乳幼児ではそのことが懸念材料となります。
では、実際の臨床現場ではどうかというと、じつは、きちんとしたデータがありません。後後方視的検討(過去のデータに基づいた研究)では抗ヒスタミン剤を服用している子の方が発熱からけいれんまでの時間が短く、発作時間も長かったという結果がでています。しかし、信頼のおける前向き検討(前に計画を立てて行う研究)はなされていません。一つだけ、差がなかったという前向き検討の報告があるのですが、対象数が少なく、もっと大規模な前方視的研究がなされないと、しっかりとしたことは言えないだろうと考えられています。ただ、理論上はまずいと考えられるので、最終結論がでるまでは、なるべく使わないでおこうということになっています。
しかし、どうしても使わざるをえない場合もあります。その場合、脳に入りにくい(脳関門を通過しにくい)第2世代の抗ヒスタミン剤がいいだろうと、これも、理論的には考えられています。ただし、実際に抗ヒスタミン剤を使うかどうかは、いろいろな要素が絡み、難しい判断を要しますので、担当医とよく相談して下さい。
キサンチン製剤(テオフィリン)は気管支喘息の急性期治療及び発症予防に使われる薬ですが、長く使うとビタミンB6の濃度を低下させることが問題視されています。ビタミンB6はけいれんを抑制する神経伝達物質GABAを作りだすための必須ビタミンですから、これが足りなくなると、やはり、けいれんが起きやすくなる恐れがあります。
しかし、抗ヒスタミン剤同様、キサンチン製剤が熱性けいれんを起こりやすくすること示すしっかりしたデータがあるわけではありません。けいれんが長引くという報告があるのですが、これついても、その後、これを確認した研究はなされておらず、最終結論がでていません。喘息の薬ですから、抗アレルギー作用を期待して、抗ヒスタミン剤も服用している子も多く、そのことも解析を難しくして、きちんとした結論をだせない原因になっています。
ただ、キサンチン製剤の濃度が高くなって、中毒域に入ると、熱がなくてもけいれんが起きやすくなることはたしかです。とくに、しばしば併用されるマクロライド系抗生物質は薬物代謝酵素シトクロームP-450 の活性を阻害してキサンチン製造の濃度を上げてしまうので注意が必要です。ですから、喘息の子の場合、キサンチンの代わりとなる薬がないか、担当医とよく相談して下さい。
このような併用薬以外に、熱性けいれんをもつ子の親御さんが心配されることに予防接種があります。この子は熱でひきつけるから予防接種ができないのではないかという相談をよく受けます。
心配の原因は2つあるようです。
一つは、予防接種の副作用で熱がでて、再びひきつけるのではという恐れです。
もう一つは、予防接種によってきわめてまれに認められる脳症が、熱性けいれんがあると起こりやすいのではないかという不安です。
しかし、いずれについても、心配はいりません。熱性けいれんがあるからといって、予防接種ができないということはありません。むしろ、熱性けいれんを起こした子こそ予防接種を積極的におこなうべきです。
たしかに、予防接種によって熱がでることがあります。そして、その熱によってひきつける危険性がないとはいえません。とくに、小児用肺炎球菌ワクチンと麻疹ワクチンは、熱がでやすいこともあって、けいれんを引き起こしやすいかもしれません。しかし、起こしやすいといっても、その頻度は0.1~0.2%で、ごくわずかです。それに、予防接種による発熱は、熱性けいれんの子にだけ出やすいわけではありません。さらに、熱が出たら、ジアゼパム坐剤でけいれんを予防すると対策も打てます。
| メモ3 百日咳のワクチンは、まず、有細胞性ワクチンが作成され、接種されました。ところが、有細胞性ワクチンは生体物質を多く含んでいたために発熱を起こしやすく、ワクチン後にけいれんを起こす子が少なからずみられました。さらに、愛知県と岐阜県で2例、ワクチン接種後に脳症となって死亡した例がみられたことから、1975年以降、百日咳ワクチンは強制接種から個別接種への移行を余儀なくされました。強制性がなくなったこともあり百日咳ワクチン接種はほとんど行われなくなりました。このため、全国で百日咳が大流行、数十名が百日咳で死亡したと推定されています。私が小児科医になった1980年前後には外来の3分の1が百日咳の子で占められ、痙攣性の咳が始まると息を止めてしまうことがあるため、赤ちゃんが次々緊急入院するといった状況になっていました。1981年、発熱を引き起こすことがまれな無細胞性(精製)ワクチンが導入され、子どもの間での百日咳の流行は鎮静しました。しかし、現在、百日咳はワクチンを打たなかった成人での流行が問題になっています。 |
最近、肺炎球菌ワクチン、ロタウイルスワクチンなどうつべきワクチンの種類が増えました。そして、そうしたワクチンをなるべく早く行うために、同時接種が増えています。いろいろなワクチンをいっぺんにうつと、副作用も相乗効果で増え、熱性けいれん再発の可能性も増えるのではないかと心配される方もいらっしゃるかもしれません。しかし、これに関しても、あまり心配する必要はありません。たとえば、従来のDPT三種混合ワクチンにインフルエンザ菌ワクチン(Hibワクチン)を同時に行った場合の熱性けいれん出現の危険性は10万人に対して4未満という報告がなされています。やはり、かなりまれです。しかも、このワクチンは3回行いますが、回を経るごとに熱性けいれんの発生頻度は下がり、3回目で発作が誘発される確率はゼロに近づきます。
つぎに、ワクチンによる脳症の問題です。
きわめてまれですが、ワクチン接種後に、けいれんが止まらなくなったり、意識が低下したりして、知能障害や運動障害が後遺症として残ったとされるお子さんがみえます。脳に何らかの変化が起きている可能性があるというので、脳症と呼ばれています。ワクチン脳症です。しかし、ワクチン脳症はきわめてまれです。100万人に1人にも満たないといわれています。
しかも、そうしたまれな「ワクチン脳症」が本当にワクチンによるものなのか、はっきりしないこともあります。
というのは、ワクチンを接種していないお子さんにも、ワクチンのあとにみられるものと同じ症状の脳症が起きているからです。つまり、ワクチン後に特徴的な臨床症状、臨床経過を示す脳症があるわけではないのです。たとえば、日本脳炎ワクチン後には急性散在性脳脊髄炎(ADEM)という、神経線維を包む髄鞘という組織がはげ落ちてしまう神経疾患がみられるとされています。しかし、ADEMは日本脳炎ワクチンを接種していない子にも発症することがありますし、その臨床症状、画像所見、臨床経過は「日本脳炎ワクチン後のADEM」と見分けがつかないことがほとんどです。日本脳炎ワクチン接種とは無関係にADEMが発症したのかもしれないのです。ワクチン脳症にはこうした「まぎれ込み」例が必ずあると考えられています。実際、ワクチン脳症は、ワクチンを接種してすぐに発症したという時間的経過以外、診断根拠がありません。しかも、ワクチン後何日以内に発症すればワクチン脳症といえるのかもわかっていなくて、したがって、定義もありません。この点もワクチン脳症というものの存在を怪しげなものにしています。ワクチン脳症というのはまれであるばかりでなく、実態がはっきりしない病態なのです。
さらに、熱性けいれんがあるからワクチン脳症になりやすいというわけでもありません。
また、最近、ワクチン脳症の存在をさらに疑わせる事実がわかってきました。
ワクチン後脳症と診断されたお子さんの血液検査をすると、神経細胞膜のナトリウムチャンネルに関与するSCN1Aという遺伝子の変異が高率にみられるという報告が相次いでいるのです。このSCN1A遺伝子変異というのは、前にも言いましたが、ドラベ症候群(乳児重症ミオクロニーてんかん)によくみられる異常です。じっさい、SCN1A遺伝子異常のあるお子さんの「ワクチン脳症」の臨床経過は、ドラベ症候群にそっくりなことが少なくありません。ドラベ症候群は、それまで、順調に発育していた赤ちゃんに発症します。たいていは、熱による遷延性けいれんが初発症状です。しかも、熱性けいれんのような高熱ではなく、38℃台の比較的低い熱で発作が起きます(お風呂にはいったときのわずかな体温の上昇で発作が誘発されることもあります)。そして、その後、長いけいれんを繰り返すようになり、ピクつきや、ボーッとする発作が日に何度も起きるようにもなります。さらに、ふらつきをはじめとして運動機能異常がみられるようになり、知的にも退行していきます。そして、ドラベ症候群のこの最初の長いけいれんが予防接種による発熱で誘発されることがありえるのです。そして、その後、けいれんを繰り返し、運動面でも知的面でも後退していくので、ワクチンをきっかけにドラベ症候群が発症したのに、ワクチンによる脳症と勘違いされる可能性があるのです。
こうした例を除くと、ワクチン後の脳症がどのぐらいになるのか、よくわかっていません。しかし、相当にまれであろうことだけはたしかです。ワクチン後の熱性けいれんとワクチン以外の発熱にともなう熱性けいれんを比較しても、てんかんを発症する確率も神経学的異常をきたす確率も変わらないことがわかっています。じつを言いますと、熱性けいれんの10%はワクチン接種の2週間以内にみられるという報告があるのですが、しかし、その発熱が本当にワクチンによるものなのか、今のように毎月のようにワクチンを行わなければならない赤ちゃんでは判断がつきかねることがあります。それに、ワクチンによる発熱だとしても、熱性けいれんの原因は発熱であって、ワクチンそのものがけいれんの原因となることはまずないと考えられています。
じつを言いますと、平成7年までは、予防接種法という法律で、けいれんを起こしてから1年以内は予防接種が禁じられていました。1970年代、種痘に関連した脳症や百日咳ワクチン後の死亡例がみられたことから、ワクチンが疑惑の目でみられるようになっていました。そうした中、なるべく、予防接種による副反応事象を見た目だけでも減らすために、熱性けいれんを含め、けいれんの既往のあるお子さんの予防接種は用心して行おうということになったのです。こうして、「まぎれ込み例」を少なくするため、最後の発作から1年間は予防接種を見合わせることになってしまいました。そのことを覚えてみえる方、あるいは、そのことをおじいさんやおばあさんなどから伝え聞いてみえる方は、熱性けいれんのある子にとって予防接種は怖いものだと感じてみえるかもしれません。しかし、その後、予防接種法が改正され、表3にあるように、そうした制限はほとんどなくなりました。
本当のところを言いますと、最後の発作からどれだけ間隔を置けば安全なのかもよくわかっていません。
一応、最後の発作から2ー3か月を開けて予防接種をすることになっていましたが、2週間も開ければ十分と判断されることもあります。それに、日に何度も発作を起こすてんかんの子がいます。そうした子は、永遠に予防接種ができないことになってしまいます。しかし、そうしたお子さんこそ、はしかや百日咳にかかった時、けいれんがさらに頻発し、大変なことになる可能性があります。ですから、その日に発作が起きていても、十分に保護者の方に説明して、予防接種をおこなうようになってきています。そうしたこともあって、最新の熱性けいれんの診療ガイドラインは「期間の提示を行わない」ことになっています。
逆にいうと、1年以上開けなければいけないというかつての方針は、確固たるデータに基づいたものではなかったのです。
どんな状態でも予防接種が大丈夫というわけでは、もちろん、ありません。しかし、熱性けいれんがあるからといって、必要以上に予防接種を恐れる必要もないのです。
| 表 3 熱性けいれんの既往がある小児の予防接種 日本小児神経学会の見解(平成15年5月) |
| 1.予防接種の実施の際の基本的事項 現行の予防接種はすべて行って差し支えない。ただし,接種する場合には次のことを行う必要がある。 保護者に対し,個々の予防接種の有用性,副反応(発熱の時期やその頻度他),などについての十分な説明と同意に加え,具体的な発熱時の対策(けいれん予防を中心に)や,万一けいれんが出現した時の対策を指導する。 2. 接種基準 熱性けいれんと診断された場合は,最終発作から2~3カ月の観察期間をおけば1.の条件のもとで接種可能である。 ただし,接種を受ける小児の状況とワクチンの種別により,主治医の判断でその期間の変更は(短縮も)可能である 長時間けいれん(15分以上発作が持続)の既往例は,小児科専門医ないし小児神経専門医が診察しその指示のもとで施行する。 3. けいれん予防策 発熱の予測される予防接種では,発熱の出現しやすい時期に発熱を認めたらジアゼパム坐剤を予防的に投与する。ただし予防投与の必要性や下記用法,用量は,主治医(接種医)の判断によって,患者ごとに変更しうる。発熱率の比較的高いのは麻疹で,時期は接種後1~12日(特に7~10日),ついでDPTでその時期は1~6日(特に1~2日)である(接種日を0日とする)。 坐薬:ジアゼパム坐薬(製品:ダイアップ座剤4mg、6mg、10mg) 用法:37.5℃以上の発熱を目安に,速やかに直腸内に挿入する。初回投与後8時間経過後もなお発熱が持続する時は,同量を追加投与してもよい。通常,2回以内の投与で終了とする。状況判断で,3回目投与を行ってもよいが,3回目は初回投与から24時間経過後とする。 坐剤がない場合はジアゼパム経口剤(製品:セルシン,ホリゾン;散,錠,シロップ)でもよい。投与量は同量で,薬物動態は坐剤とほぼ同じである。 解熱剤の併用:ジアゼパム坐剤と解熱剤の坐剤を併用する場合にはジアゼパム坐剤投与後少なくとも30分以上間隔をあける(解熱剤の坐剤の成分がジアゼパムの吸収を阻害する可能性があるため)。経口投与をする解熱剤は同時に併用してもよい。ジアゼパム投与で,眠気,ふらつき,極くまれに興奮などがみられることがある。 予防投与の必要性や用法,用量は,主治医(接種医)の判断によって変更してよい。 |
おわりに
医療関係者向けの本には、熱性けいれんの急性期の「治療」としてもっとも大切なことは、保護者の方に良好な予後も含めた熱性けいれんの一般像を口頭および(もしくは)文書で説明し,安心してもらうことだと書いてあります。何度も申してきたことですが、初めて我が子のけいれんする姿を目にした家族の方の心の動揺はかなりなものがあります。しかし、まずは、その衝撃を和らげていただくことが熱性けいれんの「治療」の第一歩となります。なるほど、まれに、細菌性髄膜炎、脳炎、乳児重症ミオクロニーてんかん、側頭葉内側硬化てんかんが熱性けいれんに隠れていることがあります。しかし、それは、たとえ複雑型熱性けいれんであっても、極めてまれです。激烈な症状からは想像できないくらい、熱性けいれんは良性の疾患です。そのことを、しつこいようですが、強調しておきたいと思います。
賢く恐れてください。
少なくとも、けいれんを恐れてお子さんの行動を制限するようなことだけは、くれぐれもなさらないでください。
参考文献
- 麻生幸三郎(1995) 側頭葉てんかん-小児科の立場から- 小児内科 27:107-115
- 高橋泉、渡辺一功,山本直樹、古根淳、麻生幸三郎ら(1987) 熱性けいれんにおける発作症状の分析. 小児科臨床 40:27-30
- 十川佳美、呉本慶子、大山昇一、高橋啓一.熱性けいれんと予防接種. 小児科臨床 64:376-9、2001
- 日本小児神経学会:熱性けいれん診療ガイドライン改定ワーキンググループ (2023).熱性けいれん(熱性発作)診療ガイドライン2023、診断と治療社、東京
https://www.childneuro.jp/modules/about/index.php?content_id=33 (2023年5月29日閲覧) - 荻原正明ら (2001) 脳波から.小児科診療 64, 326-331
- 福山幸夫、関亨、大塚親哉、三浦寿男、原美智子.熱性けいれんガイドライン.小児科臨床 49: 17-25, 1996
- 前原光夫 熱性けいれんの発作時脳波 臨床脳波 30:478-80,1988
- 山本美和、小西徹、本郷和久、八木信一、谷森正ら. 熱性けいれんの発作症状に関する検討―発作直後の家族問診票より―. 小児科臨床 49:240-244、1996
- Aso K et al (1994) Temporal lobe epilepsy of childhood onset. Jpn J Psychiatr Neurol 48: 21-220
- Baram TZ, Shinnar S ed (2002) Febrile seizures. Academic Press, Sandiego
- Berg AT, Shinnar S, Hauser WA et al (1990) Predictors of recurrent febrile seizures : a meta-analytic reviews. J Pediatr 116:329-37
- Berkovic SF, Harkin L, McMahon JM, et al (2006) De-novo mutations of the sodium channel gene SCN1A in alleged vaccine encephalopathy: a retrospective study. Lancet Neurol 5:488-492
- Bureau M(2019) Epileptic Syndromes in Infancy, Childhood and Adolescence – 6th Edition . John Libbey Eurotext, Paris,
- Caroll W, Brookfield D (2002) Lumbar puncture following febrile convulsion. Arch Dis Child 87:232-240
- Cuestas E (2004). Is routine EEG helpful in the management of complex febrile seizures? Arch Dis Child 89:290
- Curtis S, Stobart k, Bandermeer B, Simel DL, klassen T (2010) Clinical features suggestive of meningitis in children: a systematic review of prospective data. Pediatr126: 952-960
- Dube CM, Brewster AL, Baram TZ (2008) Febrile seizures: Mechanisms and relationship to epilepsy. Brain Dev 31: 366-371, 2008Heida JG, Moshe SL, Pittman QJ. The role of interleukin-1s in febrile seizures. Brain Dev 31:388-393.
- Finn A (2003). More lumbar punctures, please! Arch Dis Child 88:177
- Gordon KE, Dooley JM, Camfield PR, Camfield CS, MacSween J (2001) Treatment of febrile seizures: the influence of treatment efficacy and side-effect profile on value to parents. Pediatr 108:1080-8
- Gradisnik P et al (2015) Predictive value of paroxysmal EEG abnormalities for future epilepsy in focal febrile seizures. Brain Dev 37:868-73
- Green SM, Rothrock SG, Clem KJ et al. Can seizures be the sole manifestation of meningitis in febrile children? Paediatr 92:527-34, 1993.
- Hamelin S, Vercueil L (2014) A simple febrile seizure with focal onset Epileptic Disord 16: 112-5
- Heida JG, Moshe S, Pittman QJ (2009) The role of interleukin-1βin febrile seizures. Brain Dev 31:388-93
- Jones T, Jacobsen SJ (2007) Childhood febrile seizures: Overview and implication. Int J Med Sci 4: 110-114
- Kimia AA, Ben-Joseph EP, Prudloe T et al. (2010) Yield of lumbar puncture among children who presents with their first complex febrile seizure. Pediatr 126:62-9
- Kneen R, Solomon T, Appleton R (2002) The role of lumbar puncture in suspected CNS infection – disappearing skills? Arch Dis Child 87:181-3,
- Neville B, Gindner D (2010) Febrile seizures are a syndrome of secondarily generalized hippocampal epilepsy. Dev Med Child Neurol 52: 1151-3
- Nordli DR Jr, Moshe SL, Shinnar S, Hesdorffer DC, Sogawa Y, Pellock JM, Lewis DV, Frank LM, Shinnar RC, Sun S FEBSTAT study Team (2012) Acute EEG findings in children with febrile status epilepticus: results of the FEBSTAT study Neurology 79:2180-6
- Offringa M, Moyer VA (2001) Evidence based paediatrics: evidence based management of seizures associated with fever. BMJ 323:1111-4
- Provisional Committee on Quality Improvement and Subcommittee on Febrile Seizures (1996) Practice Parameter: the Neurodiagnostic evaluation of the child with a first simple febrile seizure. Pediatr 97:769-72
- Riordan FA, Cant AJ (2002) When to do a lumbar Puncture. Arch Dis Child 87:235-7
- Rosman NP, Colton T, Labazzo J, Gilbert PL, Gardella NB et al. (1993) A controlled trial of diazepam administered during febrile illnesses to prevent recurrence of febrile seizures. N Engl J Med 329:79-84.
- Shinnar S ed. Evaluation and management of simple and complex febrile seizures. A CME Web-Based Monograph.
- Shorvon S, Berg A (2008) Pertussis vaccination and epilepsy: an erratic history, new research and the mismatch between science and social policy. Epilepsia 49:219-25
- Steering Committee on Quality Improvement and Management, Subcommittee on Febrile Seizures. Febrile seizures (2008) Clinical practice guideline for the long-term management of the child with simple febrile seizures. Pediatrics 121: 1281-6
- Sun Y, Christensen J, Hviid A, Li J, Vedsted P, Olsen J, Vestergaard M (2012) Risk of febrile seizures and epilepsy after vaccination with diphtheria, tetanus, acellular pertussis, inactivated poliovirus, and Haemophilus influenzae type B. JAMA 307:823-31
- Subcommittee on Febrile Seizures (2012). Febrile seizures: guideline for the neurodiagnostic evaluation of the child with a simple febrile seizure. Pediatr 127: 389-394
- Takasu M et al. (2017) The semiology of febrile seizures: Focal features are frequent. Epilepsy Behav 73: 59-63.
- Bureau M (2019) Epileptic Syndromes in Infancy, Childhood and Adolescence – 6th Edition. John Libbey Eurotext, Paris Kindle 版.
- Taku T, Sugino S, Hohtani Y, Miike T (1991) Ictal EEG in febrile convulsions: a case report. Brain Dev 13:207 (abstract)
- Tarkka R, Paakko E, Pyhtinen J, Uhari M, Rantala H (2003) Febrile seizures and mesial temporal sclerosis : no association in a long-term follow-up study. Neurol 60:215-8
- Tenney JR, Schapiro MB (2012) Hemiconvulsion-hemiplegia-epilepsy syndrome. Neurology e1-e4.
- Tonia J, Jacobsen SJ (2007) Childhood Febrile Seizures: Overview and Implications. Int. J. Med. Sci. 4
- VanLandingham KE, Heinz ER, Cavazos JE, Lewis DV (1988) Magnetic resonance imaging evidence of hippocampal injury after prolonged focal febrile convulsions. Ann Neurol 43:413-26
- Verity CM, Greenwood R, Golding J (1998) Long-term intellectual and behavioral outcomes of children with febrile convulsions. N Engl J Med 338, 1723-8.
- Verity CM (1998) Do seizures damage the brain ? The epidemiological evidence. Arch Dis Child 78,78-84
- Waruiru C, Appleton R (2004) Febrile seizure: an update. Arch Dis Child 89:751-756
- Watanabe K, et al (1993) Benign partial epilepsy with secondarily generalized seizures in infancy. Epilepsia 34:635-8
- Cendes F, Sanker R (2011) Vaccinations and febrile seizures. Epilepsia 52 (Suppl 3):23-25
